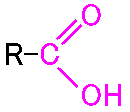

カルボン酸は、カルボニル基を持つが、その水酸基のため、いくつかの異なる性質を持つ。
OH の酸素の存在により、カルボニル部分の炭素は、あまりδ+に帯電していない。
そのため、カルボン酸は、反応性が低く、求核反応を受け難い。
分子間水素結合を、分子間で2回して、二量体になっているため、一般に沸点は高い。
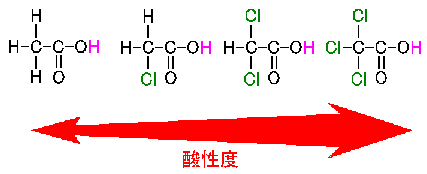
水素を塩素に置換すると、酸性度が増加する。
これは、塩素は電位陰性度が大きいため、結合した炭素を正電荷に帯電させ、カルボキシラートイオン部分から、電子を引くためである。
塩素に限らず、電気吸引性の基で置換すれば、酸性度が増加する。これを誘起効果と呼ぶ。
逆に、電子供与性基で置換すると、酸性度は下がる。
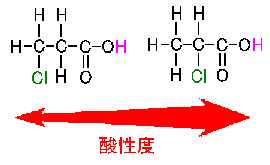
また当然、誘起効果は、離れると弱くなる。