 La composition de la
matière
La composition de la
matière
I. Les éléments
:
- Un élément est
une substance pure qui
ne peut être décomposée en substances plus
simples.
Le tableau périodique, inspiré par Mendeleïev, en donne la
liste complète.
- Sur la Terre, il existe 90 éléments naturels,
le plus léger étant l'hydrogène et le plus
lourd l'uranium. Les autres éléments ont
été fabriqués par les
scientifiques.
- On divise ces éléments en deux grands groupes
:
- a. les métaux: brillent (éclat), bons
conducteurs, malléables, ductiles, ...
Ex.: fer, cuivre, mercure, plomb, zinc, aluminium, sodium
...
- b. les non-métaux: mauvais conducteurs, non
malléables, non ductiles, ternes, ...
Ex.: oxygène, soufre, phosphore, azote, ...
Quiz sur les
éléments
II. Les composés :
- Un corps pur composé (à ne pas confondre avec
mélange ou
solution) est constitué d'atomes d'éléments
différents, groupés en molécules.
- Les propriétés d'un composé sont
différentes de celles des éléments qui les
constituent.
Ex. : H2O n'a pas les mêmes
propriétés que H2 (gaz inflammable) ou
que O2 (entretient la combustion).
NaCl a des propriétés très
différentes de Na (sodium, métal qui réagit violemment avec
l'eau) et de Cl2 (chlore, gaz jaune - vert dangereux
à respirer).
III. La molécule (Voir liaisons chimiques) :
IV. L'atome (voir la structure de):
- L'atome est la plus petite partie d'un
élément qui puisse réagir
chimiquement.
- On utilise les symboles chimiques pour représenter
les éléments et leurs atomes.
Le symbole commence par l'initiale (en majuscule d'imprimerie)
du nom international de l'élément suivie,
éventuellement, d'une deuxième lettre (en
minuscule) pour éviter la confusion.
Ex. : C = carbone; Ca = calcium; Cd = cadmium; Co = cobalt
Na = sodium (du latin natrium); K = potassium (du latin
kalium).
V. Formules :
- La molécule d'un corps simple
(élément) ou d'un corps composé est
représentée par une formule.
- Le nombre d'atomes des éléments
présents dans la molécule est indiqué au
moyen d'indices placés à droite des symboles.
Ex.: H2O = une molécule d'eau se compose de
deux atomes d'hydrogène et d'un atome
d'oxygène.
Cu(NO3)2 = une molécule de nitrate
de cuivre se compose d'un atome de cuivre, de deux atomes
d'azote et de six atomes d'oxygène.
O2 = une molécule d'oxygène
composée de deux atomes d'oxygène.
VI. Equations chimiques : Dans une
équation chimique, on indique à gauche les symboles
des réactifs et à droite ceux des produits obtenus.
La masse des réactifs doit
toujours être égale à la masse des
produits.
Ainsi, dans HCL + NaOH 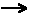 NaCl + H2O, HCl et NaOH sont les
réactifs et NaCl et
H2O sont les produits de
la réaction.
NaCl + H2O, HCl et NaOH sont les
réactifs et NaCl et
H2O sont les produits de
la réaction.
Pour mieux comprendre comment équilibrer les
équations, allez à Équation-bilan et à Stoechiométrie.
VII. Nomenclature de chimie
inorganique Cliquez ICI.
 La composition de la
matière
La composition de la
matière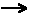 NaCl + H2O, HCl et NaOH sont les
réactifs et NaCl et
H2O sont les produits de
la réaction.
NaCl + H2O, HCl et NaOH sont les
réactifs et NaCl et
H2O sont les produits de
la réaction.