





FÍSICA E O MERGULHO - Parte 1
O Homem e o Mundo Submarino
Pode-se dizer que o homem vive entre uma superfície de um mar líquido e o fundo de um mar gasoso. O peso dessa camada gasosa sobre a superfície corporal chamamos de pressăo atmosférica, a qual o nosso corpo está adaptado. Ao aventurar-se nas incursőes submarinas, o homem enfrentou uma série de elementos adversos, conseguindo sobrepujá-los através de readaptaçőes ou do emprego de equipamentos adequados.
O AMBIENTE: No ambiente submarino, o homem tem que adaptar-se a uma série de condiçőes adversas quais sejam:
Ao nível do mar vimos que existe uma pressăo atmosférica e que quantitativamente dizemos 1 atm (uma atmosféra de pressăo).
Sendo uma atm = 1,033 Kg/cm2 = 14,7 lb/pol2 = 10 m col. H2O = 32,8 pés H2O.
Podemos considerar um arredondamento para efeito de cálculo da seguinte forma:
1 atm = 1 Kg/cm2 = 15 lb/pol2 = 10 m col. H2O = 33 pés H2O.
Usamos ainda as seguintes unidades:
1 m = 3,28 pés = 39,37 pol
1 m3 = 35,3 pés3
1 Kg = 1000 g = 2,205 lb
1 pé = 12 pol.
Converta para metros: 33, 60, 297, 165 pés.
Respostas: 33 pés = 10,0584 m.
60 pés = 18,2880 m.
297 pés = 90,5256 m.
165 pés = 50,2920 m.
Fórmulas:
Conversăo pés em metros - multiplicar por 0,3048
Conversăo metros em pés - multiplicar por 3,281
Significado das abreviaturas abaixo:
Atm = Atmosféra
P = Pressăo (medida em quantidade de atmosféras)
V = Volume (medido em litros = l)
LEIS DA FÍSICA
Lei de Boyle
"Se a temperatura permanece constante, o volume de um gás varia com a pressăo absoluta do sistema".
Pressăo absoluta - É a pressăo do sistema mais uma unidade (pressăo atmosférica).
Pressăo monométrica - É a pressăo do sistema.
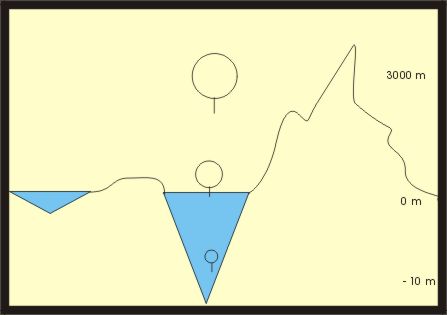
Encontramos a 10 metros de profundidade uma coluna de água de 10 metros, conseqüentemente
uma pressăo relativa a coluna de 1 atm, que somada a que existe na superfície teremos 2 Atm absolutas.
1 atm - pressăo manométrica ou relativa.
2 atm - pressăo absoluta a 10 m. (manométrica mais uma)
Sempre para efeito de cálculo usaremos a pressăo absoluta. Exemplo:
| m (profundidade) | Atm (pressăo absoluta) |
|---|---|
|
o |
1 |
|
10 |
2 |
|
20 |
3 |
|
30 |
4 |
Aplicando a Lei de Boyle: Um volume de 120 litros, na superfície -
|
a 10 m |
60 l |
|
a 20 m |
40 l |
Lei de Boyle: PV = P1V1 Exemplo:
1) Temos 100 l de um gás na superfície. Quanto teremos a 10 m de profundidade?
P = 1 Atm
V = 100 l
P1 = 2 Atm
V1 = ?
Entăo:
1 X 100 = 2 X V1
V1 = 100/2 = 50 l
2) Temos 120 l na superfície. Quanto teremos a 30 metros?
P = 1 Atm
V = 120 l
P1 = 4 Atm
V1 = ?
Entăo:
1 X 120 = 4 X V1
V1 = 30 l
Notamos ainda que a maior variaçăo fica na faixa dos 10 primeiros metros, sendo assim a mais perigosa quando falamos de volumes gasosos.
Significado das abreviaturas abaixo
PT = Pressăo Total
PP = Pressăo Parcial
N = Nitrogęnio
O = Oxigęnio
LEI DE DALTON
"A pressăo total exercida por uma mistura de gases é a soma das pressőes parciais exercidas por cada gás se ocupasse sozinho todo o
sistema".
Exemplo: Ar atmosférico - 80% de N mais 20% de O2 (em n.o arredondado)
(sistema)
pressăo do sistema = pressăo total (pt), 1 Atm.
PT = PP + P1P1
no exemplo PT = PPN + PPO = 1 Atm (80 e 20%)
PPN - 0,8 e PPO = 0,2
1) Um sistema com ar atmosférico, com 2 Atm de PT, quais as pressőes parciais deste sistema?
PPO2 = 20% da PT - 20% de 2 Atm = 0,4 +
PPN = 80% da PT - 80% de 2 Atm = 1,6
Soma será igual a 2,0
2) Quais as pressőes parciais de uma âmpola contendo ar comprimido a 150 Atm?
PPO2 = 20% da PT - 20% de 150 Atm = 30 +
PPN = 80% da PT - 80% de 150 Atm =120
Soma será igual a 150
Diver Seven Sea © 2006-2008. Todos os direitos reservados.