

電子雲にはいくつかの決まった形があります。
積乱雲とか、乱層雲とか・・・・じゃなくてね(^^)。
まずs軌道と呼ばれるタイプの電子雲があります。
これは球形をしています。
次に、p軌道と呼ばれるタイプの電子雲があります。
これは、むにょ〜と伸びた、みたらし団子(2個)のような形をしています。
さらに、d軌道と呼ばれるタイプがあります。
これはpに似ていますが、ちょっと違います。
他にもいろいろありますが、まずこの3つだけ教えておきます。
しつこいですが、この電子雲は回っていませんよ。止まっているんですよ。
で、この電子雲、s軌道、p軌道、d軌道には、一つの軌道に電子が二個まで入る事ができる性質があります。(なぜ二個なのかというのは、非常に難しいので、ここでは説明しません)
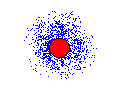
これが分かると、電子殻に入る電子の数が分かってきます。あのK殻、L殻、M殻、N殻・・・って奴です。
K殻というのは正確に説明しますと、K殻はs軌道一個でできています。
左の絵では、赤い丸は原子核を表しています。
K殻はs軌道でできているので、K殻には電子が二個入る事が出来ます。
またs軌道は、K殻だけに存在するのではないので、識別するために、1s軌道と言います。
水素とヘリウムは、1s軌道でできている、こういう状態なんですね。
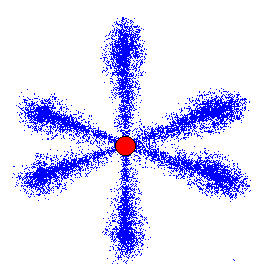
次にL殻ですが、これがちょっとややこしいです。
まず、p軌道は、s軌道と違い、同時に3個まで存在出来ます。
3個というのは、互いに直交する様にp軌道が存在できるからです。
で、L殻というのは、実は単一の殻ではなく、s軌道一個とp軌道三個でできています。正確には「2s軌道」「2p軌道」と呼びます。
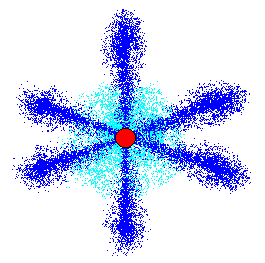
で、電子は軌道一つに二個入れますから、L殻全体としては8個の電子を収容出来ます。
左の絵では、赤丸が電子核、水色が2s軌道、青色が2p軌道を表しています。
OK?
この事を踏まえて、次のページでは、化学結合はどう考えられるかを説明しましょう。