 |
1.2- Constituant de l’atome : Un atome est constitué d’un noyau autour duquel gravitent des électrons.
I-
CONSTITUTION DE L’ATOME
1.1- Définition : L’atome est la plus petite quantité d’un élément qui puisse entrer en combinaison pour former une molécule.

1.2- Constituant de l’atome :
Un atome est constitué d’un noyau autour duquel gravitent des électrons.
1.2.1- Le noyau : Il est essentiellement formé de deux particules :
* Le proton : Il a une masse mp de 1,67.10-27 Kg et une charge électrique positive e = 1,6.10 C
* Le neutron : La masse du neutron est également supérieure à celle du proton. Il ne porte pas de charge électrique.
1.2.2- L’électron : Chaque électron porte une charge électrique négative de même valeur absolue que celle du proton. Il est plus de mille fois moins lourd que le proton.
Sa masse est :
M = mp / 1840 = 1,67.10-27 /1840 = 0,91.10-30
Kg
1.3-
Charge et masse d’un atome :
1.3.1- Charge : Dans un atome, le nombre d’électrons est égal au nombre de protons ( Z ). Il en résulte que la charge électrique totale d’un atome est nulle.
Z est appelé nombre atomique ou numéro atomique. Il correspond au nombre d’électrons ou de protons.
1.3.2- Masse : La masse de l’atome est concentrée dans le noyau. Son volume est très réduit et sa masse volumique très grande.
Remarques :
1.
Une mole d’atomes est une quantité arbitraire contenant N
= 6,02.1023 atomes réels. N
est appelé nombre d’Avogadro.
2. La masse en grammes d’une mole d’atomes est appelée masse atomique et elle est désignée par la lettre A.
Donc la masse d’un atome est le rapport qui existe entre la masse atomique et le nombre d’Avogadro.
m
= A / N
Masse atomique des principaux éléments métallurgiques
Eléments |
A |
Eléments |
A |
Eléments |
A |
Eléments |
A |
|
Aluminium |
27 |
Carbone |
12 |
Molybdène
|
96 |
Silicium |
28 |
|
Antimoine |
122 |
Chlore |
35,5 |
Nickel |
59 |
Sodium |
23 |
|
Argent |
108 |
Chrome |
52 |
Niobium |
93 |
Soufre |
32 |
|
Azote |
14 |
Cobalt |
59 |
Or |
197 |
Tantale |
181 |
|
Baryum |
137 |
Cuivre |
63,5 |
Oxygène |
16 |
Titane |
48 |
|
Béryllium |
09 |
Etain |
119 |
Phosphore |
31 |
Tungstène |
184 |
|
Bismuth |
209 |
Fer |
56 |
Platine |
195 |
Uranium |
238 |
|
Bore |
11 |
Hydrogène
|
01 |
Plomb |
207 |
Vanadium |
51 |
|
Brome |
80 |
Magnésium
|
24 |
Potassium |
39 |
Zinc |
65 |
|
Cadmium |
112 |
Manganèse
|
55 |
Sélénium |
79 |
Zirconium |
91 |
II
- REPÉRAGE DES DIRECTIONS ET PLANS CRISTALLOGRAPHIQUES DE DENSITÉ
MAXIMALE
2.1 – Direction cristallographique de densité maximale :
D.C.D.M.
Une D.C.D.M. est une direction le long de laquelle les atomes sont tangentes entre eux.
2.2 – Plan cristallographique de densité
maximale : P.C.D.M.
On appelle P.C.D.M. un plan qui passe par trois atomes non alignés du réseau. Il contient au moins deux D.C.D.M. sécantes entre elles.
 |
 |
Pour une maille cubique centrée, les D.C.D.M. sont au nombre de quatre :
Remarque : Les DCDM contiennent toute l'atome centrale de la maille cubique centrée.
Les Plans C.D.M. sont au nombre de six :
2.4 – Cas d’une maille cubique à faces centrées :
Pour une maille
cubique à faces centrées, le nombre de D.C.D.M. est de six :
(2,4) ; (2,7); (4,7); (1,3); (1,6); (3,8)
Deux directions // sont considérées confondues
 |
 |
Les P.C.D.M. sont au nombre de huit :
 |
 |
Pour une maille compacte, le nombre de D.C.D.M. est de trois.
Les P.C.D.M. sont au nombre de quatre et correspondent aux plans de base de l’hexagone
III
– DÉTERMINATION DU DIAMÈTRE
DES ATOMES
Pour la détermination du diamètre, nous considérons pour chaque cas le P.C.D.M.
3.1
– Maille cubique centrée
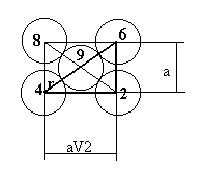
Considérons le P.C.D.M. (2-6-8-4 ) et soit le triangle 4-2-6. Calculons le diamètre
de l’atome.
.………………………………………………………………………………………………………………………………………………………………………………………………………………………….…………………………………………………………………………………………………………….…………………………………………………………………………………………………………….…………………………………………………………………………………………………………….
3.2
– Maille cubique à faces centrées :

Soit le P.C.D.M. ( 2-7-4 ). Calculons le diamètre de l’atome.
.………………………………………………………………………………………………………………………………………………………………………………………………………………………….…………………………………………………………………………………………………………….…………………………………………………………………………………………………………….…………………………………………………………………………………………………………….
3.3
– Maille hexagonale compacte

Soit la base hexagonale (1-2-3-4-5-6 ) , calculons le diamètre de
l'atome
.………………………………………………………………………………………………………………………………………………………………………………………………………………………….…………………………………………………………………………………………………………….…………………………………………………………………………………………………………….…………………………………………………………………………………………………………….