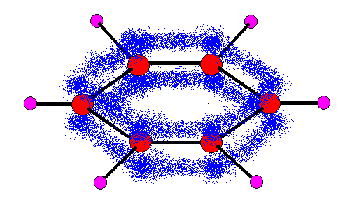

まず結論から書きますと、ベンゼンの構造は右のような構造になっています。
ここでこの絵から、いくつか重要な事が分かります。
ベンゼンは図の通り、平べったい平面構造を採っています。
全ての結合は「二重結合と単結合の中間状態」と書きましたよね。単結合ならSP3混成軌道ですから、正四面体構造を採るはずです。が、そうはなっていない訳です。どっちかというと、二重結合で使われるSP2混成軌道と同じ、平面構造を採っている訳です。

「それがどうした(何が特別なんだ?)」
と思いますでしょ。
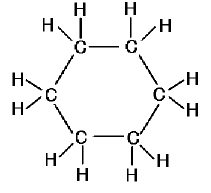
じゃあ、ベンゼンと似ているけど違う、C6H12を考えてみましょう。
右側にC6H12の構造の一例を示しました。(実は他のタイプもあります)
C6H12は水素の数が違うだけでなく、形が全然違ってくる。だって単結合だから、SP3混成軌道で平面構造にならないんです。
どっちかといえば、こっちの方がよくあるタイプでして、むしろベンゼンの様な平面構造の方が特別なんですね。
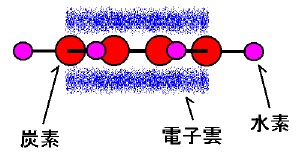
これもSP2混成軌道の影響ですが、構造の上下をπ電子がサンドイッチしている構造になっています。
電子ですから負電荷を持っています。つまりベンゼンは表面が負電荷でコーティングしてある状態なのです。
ということは、周りに負イオンが飛んできても跳ね返してしまい、ベンゼン本体に接近する事が出来ず、反応を起こせません。
結果として、ベンゼンはすごく安定した構造になります。
アルケンのところで書きましたが、二重結合というか、π結合は本来反応性に富んでいて、付加反応を起こし易いものです。
ベンゼンもπ結合を持っているのですから、本来付加反応をし易そうなものです。しかし実際には付加反応をめったに起こしません。
ベンゼンは付加反応よりもむしろ置換反応を起こします。
ともかく基本的には、ベンゼンは反応をし難いんです。
だからベンゼンはそれ自身が一つの基として行動するんです。
環状炭化水素:独学ための有機化学の「次のページ」へ:独学ための有機化学へ:目次へ