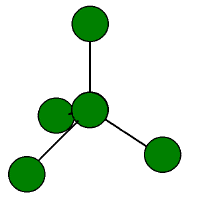

周期表で、炭素の下である事から分かる通り、炭素と性質が似ている面が多い。
周期表から分かる通り、金属と非金属の中間に位置し、半導体である。そのため結晶は金属光沢を持つ。(色は青緑がかった黒)
半導体なので、工業的に重要。
化学的には安定している。塩基には侵され、ケイ酸塩になる。
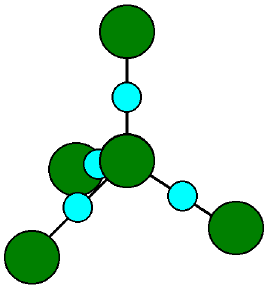
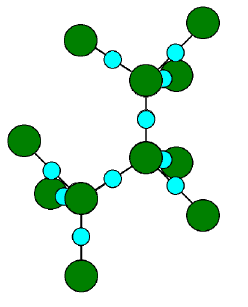
天然には、二酸化ケイ素SiO2として存在する。
構造はダイヤモンド構造である純粋なケイ素に、酸素が割り込んだ形。(左の図:緑はケイ素、水色が酸素)(右の図:左の図がこんな感じで繋がって、巨大分子になる)
二酸化ケイ素は、早い話が「ガラス」や「石コロ(石英やケイ砂)」の主成分。
純粋なケイ素は、二酸化ケイ素をコークスで還元して得る。
純粋な二酸化ケイ素の結晶は、いわゆる「水晶」の事。光学機器に利用される。
二酸化ケイ素もケイ素同様、安定であるが、フッ化水素に溶ける。(重要)
二酸化ケイ素はダイアモンド型共有結合結晶として有名。
融点は非常に高い(1713℃)。
塩基の共存のもと加熱すれば、融解してケイ酸ナトリウムNa2SiO3になる。これに水を加えると、水アメ状の「水ガラス」になる。さらにこれに濃硫酸を加えると、白いノリ状に固まる。これをケイ酸H2SiO3と言い、乾燥させたものが乾燥剤シリカゲルである。