
窒素と同族元素だが、化学性質はかなり異なっている。
同素体として黄リンと赤リンがある。
赤リンは現在のマッチ箱の側面に塗ってある、赤茶色の部分。
分子式はP4。
不安定で、自然発火(発火点60℃)するため、水中に保存する。
猛毒。
昔はマッチに使われていたが、危険なため、現在は赤リンを利用している。
ロウ状、特異臭。暗所で青白く発光する。
二硫化炭素CS2に可溶。
鎖状高分子。
黄リンと違い、無臭、無毒。
発火点は260℃で、自然発火しない。
現在のマッチ箱の側面に塗ってある、赤茶色の部分。(マッチの先っぽは硫黄)
二硫化炭素CS2に不溶。
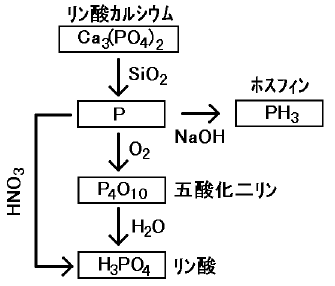
リンは天然に遊離の状態で産出する事はない。それはリンが酸素と化合する性質がはなはだ強いからである。リンの工業的な製造法としては、リン酸カルシウムをその半分のコークスおよびケイ砂と混合し、電気炉内で強熱する方法がある。ここでリンは蒸気として発生するから、この蒸気を空気と触れないように水中に 導いて凝縮させる。こうして得られるリンを黄リンと言う。この黄リンを空気を遮断した密閉容器内で長時間250℃付近で加熱すれば赤リンになる。黄リンと赤リンは同素体である。色、比重、融点などの物理的性質が違う他、赤リンは空気中でも安定であるのに対し、黄リンは空気中で発火する危険性を持つなど化学的性質も大きく違っている。また黄リンはニラの様なにおいがして猛毒であるのに対し、赤リンはにおいも毒性もないというように生体に対する作用も異なっている。リンは燃焼させれば白色粉末状の五酸化二リンになり、ここで生成した五酸化二リン過剰の水と反応させればリン酸になる。リン酸は3価の酸であるので、アルコール類との反応では結合するアルコールの数により3種類の化合物を生じる。この化合物は広い意味のエステルと考えることができる。
[京都府立医科(赤字出題時空欄)]
リン酸カルシウムから、リン単体を生成する反応はこれ。
SiO2を使って、リン酸カリからP4O10を遊離させて、コークスで還元して得る。
順位 |
国名 |
比率 |
1 |
アメリカ合衆国 |
33.2% |
2 |
中国 |
16.0% |
3 |
モロッコ |
15.4% |
4 |
ロシア |
6.7% |
5 |
チュニジア |
5.5% |
|---|
順位 |
国名 |
比率 |
1 |
アメリカ合衆国 |
33.7% |
2 |
中国 |
15.4% |
3 |
インド |
7.8% |
4 |
ロシア |
5.2% |
5 |
ブラジル |
4.2% |
|---|