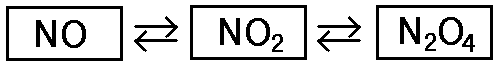

二酸化窒素と違い無色無臭。
非常に酸化され易い。結果として二酸化窒素になる、
参加され易いので、還元力が有る。
一酸化窒素NOは、生体内で神経伝達物質として働くなど意外な役割を果たしている。このNOを実験室で簡単に発生させるには、銅に希硝酸を作用させ、水上置換で集める。また工業的には、アンモニアを空気中の酸素と800℃で白金を触媒として反応させて、製造する。
[慶應95医]
ちなみに、「なぜ水上置換するのか」が問題になっていましたが、一酸化窒素は水と反応し難いのと、空気中で下方置換すると、空気中の酸素と反応して、二酸化窒素になってしまうからでしょう。
また、本文で指摘されている実験室的・工業的製法を、化学反応式で書けという設問もありましたが、
実験室的:3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
工業的:4NH3 + 5O2 → 4NO + 6H2O
でしょう。