では、そもそもなぜ、凝固点降下が起きるのでしょう?
これは、こんな風に考えれば分かり易いでしょう。
まず理科のお話で書きましたように、「自然は無秩序を好む」という事に注目します。
共鳴理論を読んで下さい。
これを踏まえて、砂糖水を凍らせる事を考えましょう。
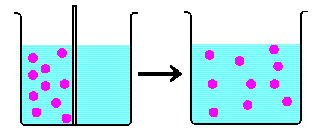
まず凍る話の前に、この様な状態を考えて下さい。
ビーカーに板を入れて、半分に仕切り、片方に砂糖を溶かします。
この状態で仕切り板をはずすと、砂糖分子が分散して、一定濃度の砂糖水が出来ますね。
この状態から、再び仕切り板を入れても、元の状態には戻りませんね。
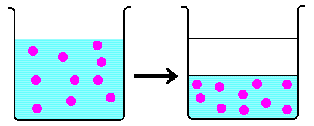
つまりこの過程は不可逆過程なのです。
つまり逆向きの操作は、すごく不自然な操作なんですね。
この事を踏まえて、砂糖水の凍る様子を考えてみましょう。
砂糖水が凍っても、氷の中には砂糖は含まれませんよね。
という事は、仮に砂糖水が半分凍ったとしたら、砂糖分子が漂う事ができる体積(液体部分)の体積が半分になります。ですから砂糖水の濃度が倍になる訳です。
これはすごく不自然な動作です。ですから砂糖水は、純粋な水より凍りにくい訳です。
ですから、0℃位では凍りません。
その砂糖による凍り難さより、凍る強さを強くするために、もっと温度を下げてやる必要があります。だから砂糖水を凍らせるためには、-2℃とか-3℃にする必要があります。
これが、凝固点降下の簡単な理由です。