
コップをかぶせた方は、蒸発が起きない訳ではありません。
蒸発は起きるけれど、水はなくならないんです。
蒸発した水は、コップの中に漂う事になりますよね。
しかし理科のお話7で書きましたように、コップの中に漂う水の量には限界があります。中学校の理科では、1m3あたりに溶けられる水のg数でその限界量を表しましたね。それを「飽和水蒸気量」と呼びました。
でもそもそも、なぜ「限界量」があるんでしょう?
それは結局、「平衡」の考え方に行き着きます。
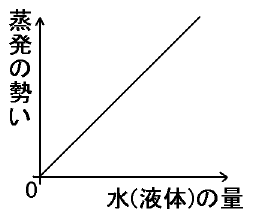
「水が蒸発する勢い」は、当然「水の量」に比例します。
言い換えれば、(厳密性は失いますが)「水が蒸発する量」は、水の量に比例します。
コップの中の水も、初めは勢い良く蒸発しますが、蒸発に伴い(実際には、微量にですが)量が減り、蒸発の勢いが落ちます。
さらに、この理屈は、コップ内部に充満する水蒸気にも通用します。
蒸発した水は、水蒸気としてコップ内部に溜まっていきますから、「充満する水蒸気としての水の量」は次第に増加します。
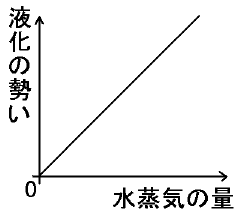
さらに、「水蒸気」も偶発的にある確率で、水に戻る奴います。
当然、「水蒸気が水に戻る勢い」は、水蒸気の量に比例します。
言い換えれば、(厳密性は失いますが)「水蒸気が水に戻る量」は、水の量に比例します。
つまりコップの中の水は、蒸発に伴って、気化の勢いが減速し、液化の速度が加速します。
ならば、「ある量」だけ蒸発すると、「気化の速度」と「液化の速度」が釣り合いませんか?だって「水の量+水蒸気の量」は一定なんだから。
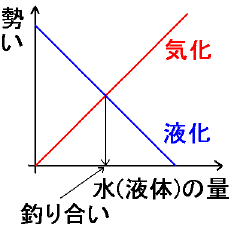
早い話が平衡状態(釣り合い)に至る訳です。
(右側の図で、「液化の勢い」のグラフが「右下がり」なのは、横軸が「液体の水の量」だからです。液体の水が多いという事は、気体の水(水蒸気)が少ないという事ですから、「水蒸気の液化」のグラフは左右反対にする必要があるため、こうなっています。)
ですから、コップをかぶせた方は、水が全て蒸発して無くなるという事はありません。
まずここまでは良いでしょうか?
ここまで分かったら、次のページでは、このグラフから分かる他の情報について説明しましょう。