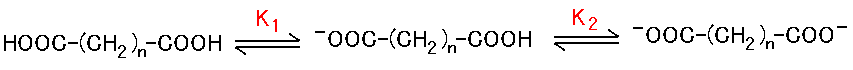
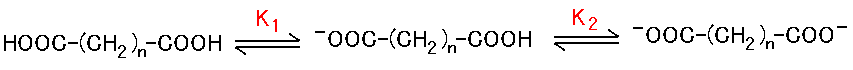
カルボキシル基が二つあるので、解離定数は当然二つある。
第一解離定数 Ka は、酢酸の解離定数よりも、必ず大きな値を持つ。
すなわち、酸が強いという事だ。
理由は、第一電離によって生じたモノカルボキシラートイオン -OCC-(CH2)n-COOH の負電荷が、残っているカルボキシル基によて安定化されるため、ジカルボン酸のモノカルボキシラートイオンは、モノカルボン酸のカルボキシラートイオンよりも安定だからである。
「安定化」の理由は、いろいろな説明があるが、カルボキシル基が電子吸引性である事や、共鳴による、電子の非局在化などが挙げられる。
残っているカルボキシル基が鍵なので、当然 Ka が上がる効果は、カルボキシル基同士が近接しているほうが、つまりnが小さいほうが大きい。
逆に、Kb は、酢酸の解離定数よりも小さい。
それは、解離後のジカルボキシラートイオンは、負電荷を2つ持ち、不安定になるからである。