光学異性体
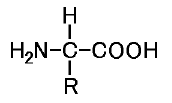
構造を見て分かりますように、(グリシンだけは例外ですが)アミノ酸は必ず不斉炭素原子を持っている事になりますね。ですから光学異性体が存在します。
分子内塩と双性イオン
アミノ酸の構造は、おもしろい形をしていませんか?
カルボキシル基は酸性で、アミノ基は塩基性です。分子内に酸と塩基の両方が存在している訳です。
という事は、アミノ酸を水に溶かすと、分子内中和が起きまして、
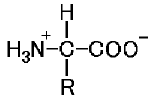
という塩になります。この様な「分子内塩」を「双性イオン(両性イオン)」と言います。
じゃあ、中性の水ではなく、酸性or塩基性の水に溶かしたら、この双性イオンはどんな状態を採るのでしょうか?
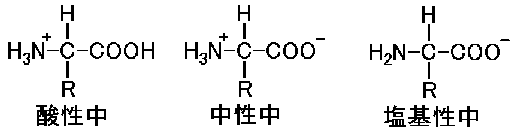
結論はこうなります。酸性中では、H+が過剰に存在しますから、カルボキシルイオンが塩基として働いて、そのH+を受け取り、逆に塩基性中ではH+が不足していますから、アミノ基イオンが酸として働き、H+を放出します。
等電点
もう一度、双性イオンの構造を見てください。
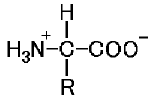
電荷自身は存在しますが、分子内に正・負の両方が等量存在します。ですから分子全体としては、電荷を持っていないとの同じですね。
この状態で、この双性イオンが溶けている水溶液に電極棒を突っ込んで電圧を掛けても、どちらの極にも引き付けられません。
ところが酸性中で同じ事をやると、事情が異なります。
上の図から分かりますように、酸性中ではアミノ酸は正電荷を持っている事になりますから、負極に引き付けられます。
逆に塩基性中では、負電荷を持っている事になりますから、正極に引き付けられます。
ところでここで問題になりますのが、「中性とはなんぞや」という事です。
中性では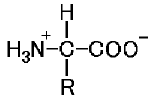 の構造になるとは書きましたが、それはそうなんですが、それがPH7での話とは限らないんです。
の構造になるとは書きましたが、それはそうなんですが、それがPH7での話とは限らないんです。
具体的に書きますと、グルタミン酸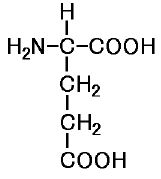 はPH3.2の時、丁度電荷を持たない状態になります。そしてPH3.2を下回る時に、酸性型のイオン(正に帯電した状態)になり、PH3.2を越える時に、塩基性型のイオン(負に帯電した状態)になります。
はPH3.2の時、丁度電荷を持たない状態になります。そしてPH3.2を下回る時に、酸性型のイオン(正に帯電した状態)になり、PH3.2を越える時に、塩基性型のイオン(負に帯電した状態)になります。
このグルタミン酸の場合、PH3.2では、電荷が無い状態です。この様に電荷が無い状態になるPHを、「等電点」と言います。グルタミン酸の等電点はPH3.2です。
等電点はアミノ酸の種類によって異なります。例えばリシンなんかはPH9.4が等電点になります。
ですからこの性質を利用すると、アミノ酸を分析できます。
よくやる方法では、こうやります。
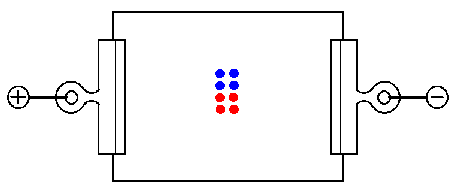
水を染み込ませた「ろ紙」を用意して、二個所の端をクリップではさみます。そこに電池を繋いで電圧を掛けます。(物理を採っている人に、正確に言うと、電場・電界を作った訳です)
ろ紙に染み込ませた水のPHは、必要に応じて調整しますが、今回はPH7にしている場合で説明します。PH5でやるときは例えば炭酸を、PH9でやる時は例えばアンモニア水を加えて調整します。今回はPH7ですから、何も加えません。
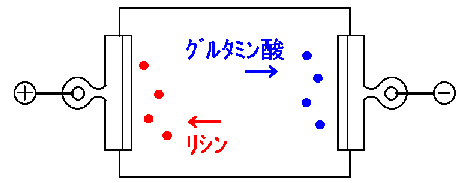
この状態で、ろ紙の中央に、「グルタミン酸+リシン混合液」を一滴たらして、しばらく様子を見ましょう。
PH7ですから、グルタミン酸はマイナスに帯電していますから、正極付近に集まりますし、リシンはプラスに帯電していますから、負極付近に集まります。
電気泳動の応用ですね。
この方法で、PHを調整しながら実験を繰り返す事で、もともとの混合液には、どんな種類のアミノ酸が溶けていたかを調べる事が出来ます。
そんな事をして何の意味があるのかは、タンパク質を学ぶと分かると思います。