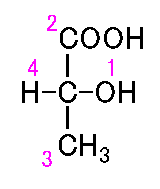
光学異性体を区別する方法。
例えば、最も易しい例として、乳酸の光学異性体を考えましょう。
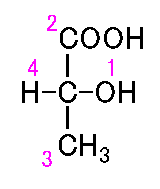
乳酸にはキラル中心(=不斉炭素原子)*が一つありますから、光学異性体を持っています。
この二つを区別するため、名前をつける必要があります。
その手順は以下の通り。
キラル中心に直接結合している原子に、番号を振ります。
番号の振り方は、
という規則があります。
乳酸の場合、水酸基の酸素が一番大きいので、これが一番です。
また、水素は一番軽いので、四番です。
問題は、カルボキシル基とメチル基です。
どちらも炭素ですから、それでは順番に差が付きません。
そこで、その炭素に結合した原子に注目します。
カルボキシル基は、直接酸素が二つ付いています。実はこれは「三つ」と数えます。なぜなら、片方の酸素は、二重結合を介して結合していますから、ニ倍して数えるというルールがあるからです。
一方、メチル基は単に水素が三つあるだけです。
そこで、カルボキシル基の順位のほうが高いと考え、こちらを二番、メチル基を三番と数えます。
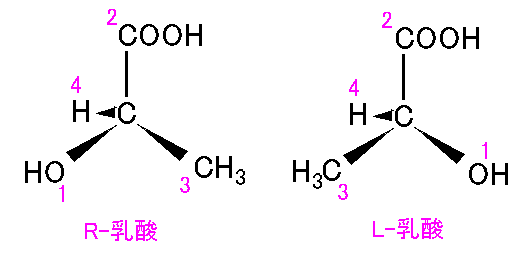
番号が振れたら、一番番号が小さい原子を、紙面の向こう側に持っていきます。
そうして手前に来る三つの原子の順位に注目します。
数字が右回りに並んでいたらR型、左回りならL型と命名します。
こうする事で、光学異性体を区別する事が可能となります。
注意:正確には「キラル中心」が必ずしも「不斉炭素原子」ではありませんが、大学受験の範囲では、ほぼ言えるでしょう。