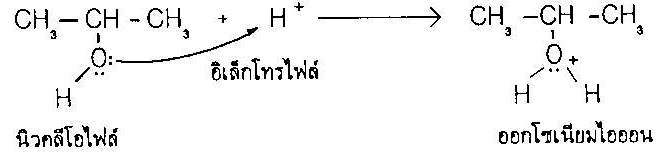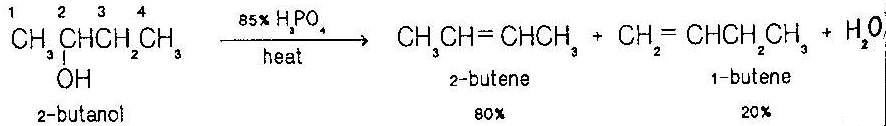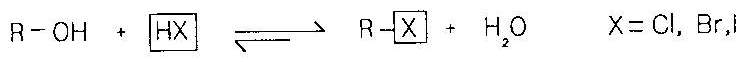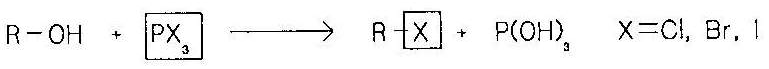|
ปฏิกิริยาของแอลกอฮอล์ |
|
แอลกอฮอล์สามารถเกิดปฏิกิริยาได้หลายแบบ เช่น ปฏิกิริยาการเปลี่ยนให้เป็นอัลคิลแฮไลด์ ปฏิกิริยาการขจัดนํ้า ปฏิกิริยาออกซิเดชัน และอื่นๆ จึงกล่าว ได้ว่าแอลกอฮอล์เป็น สารตั้งต้นในการสังเคราะห์สารประกอบต่างๆ ได้มากมาย |
|
| เมื่อพิจารณาปฏิกิริยาของแอลกอฮอล์พบว่าปฏิกิริยาของแอลกอฮอล์พบว่าปฏิกิริยาหลักประกอบด้วยการแตกพันธะ C-O และ O-H ดังนี้ | |
|
1) ปฏิกิริยาที่เกิดจากการแตกพันธะ O-H |
|
|
ก. ปฏิกิริยากับโลหะ |
|
|
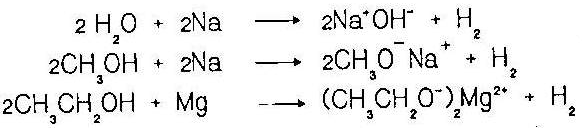
ปฏิกิริยานี้เกิดขึ้นเมื่อปฏิกิริยาของนํ้า คือ โปรตอนของแอลกอฮอล์ถูกดึงไปด้วย โลหะ เช่น ลิเทียม โซเดียม โพแทสเซียม แมกนีเซียม ให้แก๊สไฮโดรเจนและโลหะแอลคอกไซด์ ที่มีสมบัติเป็นเบส |
|
|
|
|
|
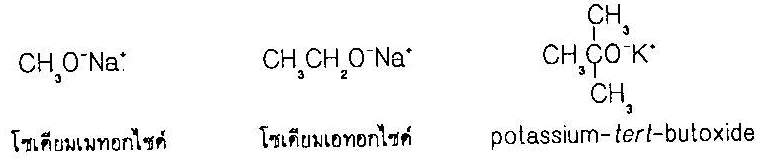
นิยมใช้แอลคอกไซด์ต่อไปนี้ เป็นเบสแก่ในปฏิกิริยาที่ไม่ใช้นํ้าเป็นตัวทำละลาย |
|
|
|
|
|
ข. การเกิดเอสเทอร์ |
|
|
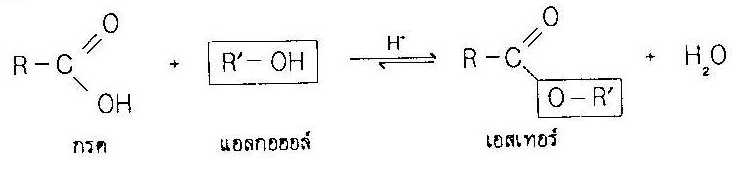
เมื่อแอลกฮฮอล์ทำปฏิกิริยากับกรดอินทรีย์และมีกรดอนินิทรีย์อยู่ด้วยจะให้ผลผลิตเปนเอสเทอร์ ซึ่งเป็นสารประกอบที่มีความสำคัญในทางชีวเคมี เป็นตัวทำให้เกิดรส กลิ่น |
|
|
สมการทั่วไป |
|
|
|
|
|
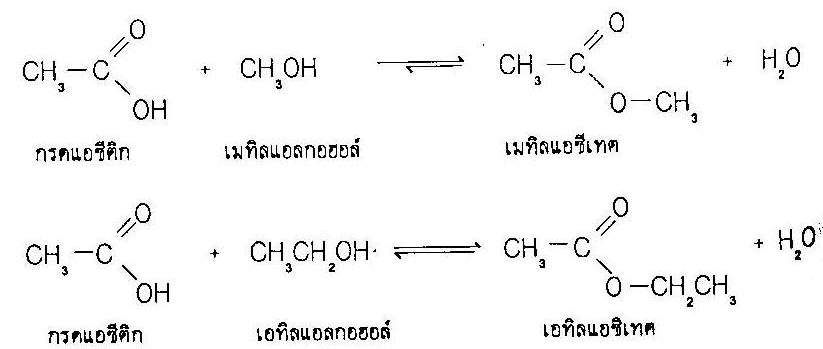
ตัวอย่าง |
|
|
|
|
|
2) ปฏิกิริยาที่เกิดจากการแตกพันธะ C-O |
|
|
ก. ปฏิกิริยาการขจัดนํ้าเมื่อมีกรดเป็นตัวเร่ง |
|
|
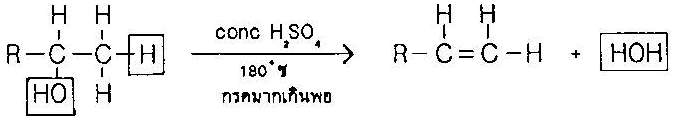
แอลกอฮอล์ถูกเปลี่ยนให้เป็นอัลคีนโดยปฏิกิริยาการขจัดนํ้า ในห้องปฏิบัติการทำปฏิกิริยาโดยให้ความร้อนแอลกอฮอล์กับ กรดฟอสฟอริก 85 % หรือกรดซัลฟิวริก |
|
|
สมการทั่วไป |
|
|
|
|
|
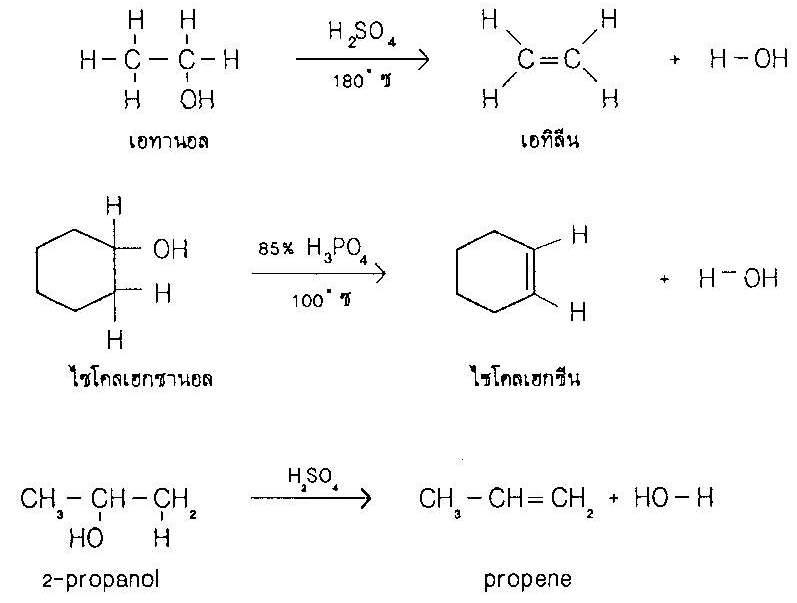
เช่น การสังเคราะห์เอทิลีนจกเอทานอล ไซโคลเฮกซีนจากไซโคลเฮกซานอล และ propene จาก 2-propanol |
|
|
|
|
|
ปฏิกิริยานี้มีการแตกพันธะซิกมา 2 พันธะ คือ C-H และ C-OH แล้วมีการก่อพันธะใหม่ 2 พันธะคือ พันธะไพ 1 พันธะ (C=C) และพันธะซิกมา 1 พันธะซิกมา 1 พันธะ (H-OH) ตามลำดับดังนี้ |
|
|
ขั้นตอนที่ 1 ออกซิเจนของแอลกอฮอล์ทำหน้าที่เป็นนิวคลีโอไฟล์ก่อพันธะซิกมากับโปรตอนของกรดที่ใช้ ให้ออกโซเนียมไอออน (oxonium ion) |
|
|
|
|
|
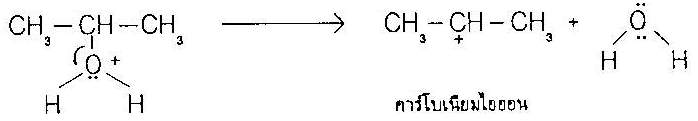
ขั้นตอนที่ 2 มีการแตกพันธะ C-O ให้คาร์โบเนียมไอออนและนํ้า |
|
|
|
|
|
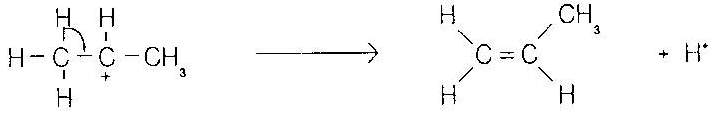
ขั้นตอนที่ 3 มีการแตกพันธะ C-H ของคาร์บอนที่ก่อพันธะกับคาร์โบเนียมไอออน (อัลฟาคาร์บอน) โดยไฮโดรเจนหลุดออกในรูปของโปรตอน เป็นการสร้าง พันธะไพ ให้อัลคีน |
|
|
|
|
|
ในกรณีที่มีคาร์บอนที่ก่อพันธะกับคาร์โบเนียมไอออน (อัลฟาคาร์บอน) มากกว่า 1 ตำแหน่งจะให้ผลผลิตผสมที่เป็นไอโซเมอร์กัน เช่น เมื่อทำปฏิกิริยากา รขจัดนํ้าของ 2-butanol ให้ผลผลิตผสมของ 1-butene และ 2-butene ที่เป็นเช่นนี้เนื่องจาก มีอัลฟาคาร์บอน 2 ตำแหน่งคือ ตำแหน่งที่ 1 และ 3 เมื่อมีการแตก พันธะ C-H ของคาร์บอนตำแหน่งที่ 1 ให้ 1-butene และ ตำแหน่งที่ 3 ให้ 2-butene โดย 2-butene เป็นผลผลิตหลัก (อัลคีนที่มีหมู่แทนที่ที่พันธะ คู่มากจะเกิด มากกว่า กฎของเซย์ทเซฟฟ์ (Saytzeff's rule) |
|
|
|
|
|
ข. ปฏิกิริยาการเปลี่ยนให้เป็นอัลคินแฮไลด์ |
|
|
เราสามารถเปลี่ยนแอลกอฮอล์ให้เป็นอัลคินแฮไลด์ โดยทำปฏิกิริยากับกรดไฮโดรคลอริกไฮโดรโบมิก หรือไฮโดรไอโอดิก เรียกปฏิกิริยาที่เกิดขึ้นนี้ว่า ปฏิกิริยาการแทนที่ด้วยแฮโลเจน เกิดเนื่องจากแฮโลเจนเข้าไปแทนที่หมู่ไฮดรอกซิลของแอลกอฮอล์ |
|
|
สมการทั่วไป |
|
|
|
|
|
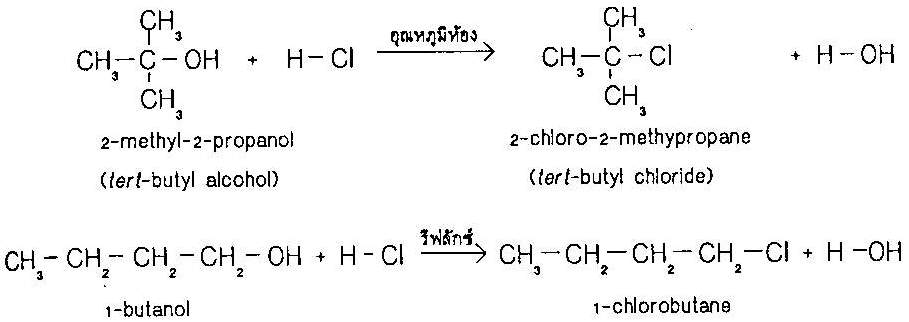
พบว่าแอลกอฮอล์ตติยภูมิจะทำปฏิกิริยาได้เร็วกว่าทุติยภูมิและปฐมภูมิตามลำดับ เช่น เมื่อผสม 2-methyl-2-propanol (แอลกอฮอล์ตติยภูมิ) กับกรดไฮโดรคลอริก ให้ 2-chloro-2-methylpropane ภายใน 2-3 นาทีที่อุณหภูมิห้อง ขณะที่เมื่อนำ 1-butanol (แอลกอฮอล์ปฐมภูมิ) มาทำปฏิกิริยาต้องรีฟลักซ์ กรดไฮโดรคลอริกจึงจะให้ 1-chlorobutane ทั้งนี้เป็นเพราะปฏิกิริยาเกิดผ่านกลไกแบบ SN1 |
|
|
|
|
|
นอกจากนี้หมู่ไฮดรอกซิลของแอลกอฮอล์ยังถูกแทนที่ได้ด้วยฟอสฟอรัสไตรแฮไลด์ เช่น PCl5 , PBr3 , Pl3 |
|
|
สมการทั่วไป |
|
|
|
|
|
และไทโอนิลคลอไรด์ (SOCl2) โดยมีกรดไฮโรคลอริกและแก็สซิลเฟอร์ไดออกไซด์เป็นผลผลิตข้างเคียง |
|
|
สมการทั่วไป |
|
|
|
|
|
3) ปฏิกิริยาออกซิเดชัน |
|
|
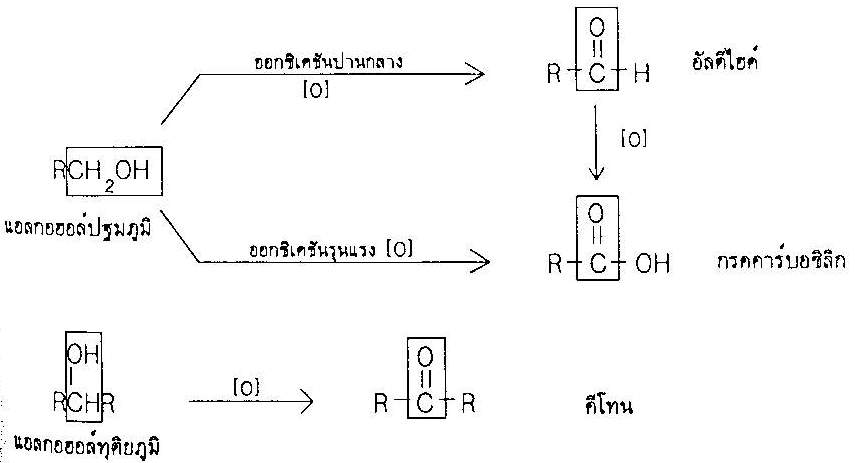
เป็นปฏิกิริยาการกำจัดไฮโดรเจนจากคาร์บอนและออกซิเจนที่อยู่ติดกันของแอลกอฮอล์ |
|
|
ให้คาร์บอน-ออกซิเจนพันธะคู่คือ อัลดีไฮด์ หรือคีโทน ขึ้นกับชนิดของแอลกอฮอล์ โดยแอลกอฮอล์ปฐมภูมิให้กับอัลดีไฮด์หรือกรดคาร์บอกซิลิก (ถ้าใช้ภาวะรุนแรง) แอลกอฮอล์ทุติยภูมิให้คีโทน |
|
|
ปฏิกิริยานี้อาจทำได้โดยใช้สารเคมี เช่น ตัวออกซิไดส์ต่างๆ หรือโดยการทำปฏิกิริยาการกำจัดไฮโดรเจนโดยมีตัวเร่ง (catalytic dehydrogenation) ดังนี้ |
|
| ก. ปฏิกิริยาออกซิเดชันโดยใช้ตัวออกซิไดส์ | |
|
สมการทั่วไป |
|
|
|
|
|
ตัวออกซิไดส์ปานกลาง คือ โครมิกออกไซด์ในไพริดีน (CrO3 / pyridine) , โพแทสฌซียมเปอร์แมงกาเนตในไดเมทิลซัลฟอกไซด์ (KMnO4 , DMSO) |
|
|
ตัวออกซิไดส์รุนแรง คือ สารละลายด่างของโพแทสเซียมเปอร์แมงกาเนต (KMnO4) , สารละลายนํ้าของโพแทสเซียมไดโครเมต (K2Cr2O7) |
|
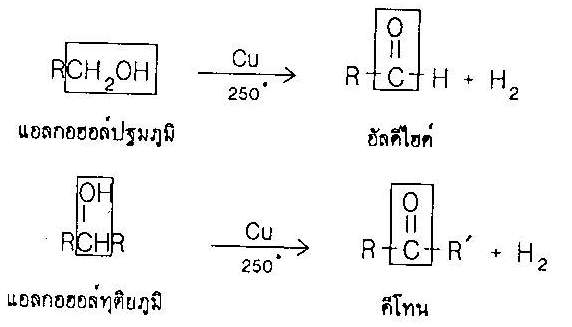
| ข. ปฏิกิริยาการกำจัดไฮโดรเจนโดยมีตัวเร่ง | |
|
|
|
| สมการทั่วไป | |
|
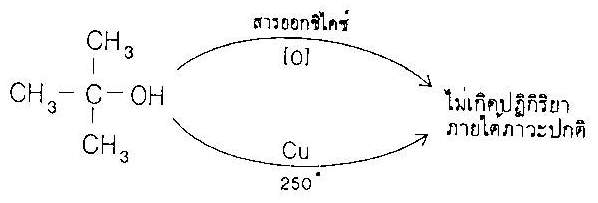
สำหรับแอลกอฮอล์ตติยภูมินั้น ไม่ว่าจะออกซิไดส์แบบใดก็ไม่เกิดปฏิกิริยา |
|
|
|
|
|
หมายเหตุ เครื่องหมาย [O] หมายถึง ปฏิกิริยาออกซิเดชัน โดยไม่จำเพาะเจาะจงรีเอเจนต์ |
|
|
ตัวอย่าง |
|
|
|
|
|
ถ้าใช้กรดเป็นกรดไฮโดรโบรมิกหรือไฮโดรคลอริก ต้องทำที่อุณหภูมิสูงกว่าปกต ิเพราะทั้งโบรไมด์และคลอไรด์ไอออน เป็นนิวคลีโอไฟล์ที่ไม่ดี ีนักเมื่อเทียบ กับไอโอไดด์ไอออน |
|