Difusión
Por: Juan Carlos
Bello Cortés
22
de mayo de 2000
El interés de las investigaciones científicas radica
en conocer el comportamiento o los procesos de las sustancias: reactivos, mezclas,
etcétera; por lo tanto es particularmente importante el comprobar experimentalmente
tales procesos o hechos. En esta ocasión nuestra problemática residió en la comprobación
y observación (detallada) del proceso de difusión: que teóricamente
nos dice que es "el movimiento de las moléculas de una región de alta concentración
a otra de menor concentración", para lo cual se tomó en cuenta que existen varios
tipos de difusión como lo son la ósmosis y la diálisis.
La intención fue la de comprobar experimentalmente
o mejor dicho verificar el efecto de la ósmosis con una membrana semipermeable
como lo es la de huevo en diferentes fluidos o sustancias en las cuales lo incorporamos,
estas sustancias son: Ácido acético, solución de glucosa y agua destilada.
Se define la Difusión como el movimiento de las
moléculas de una región de alta concentración a otra de menor concentración, producido
por la energía cinética de las moléculas (figura 1.1). La velocidad de Difusión
es una función del tamaño de la molécula y de la temperatura.
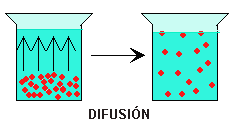
Figura 1.1
Velocidad de difusión. En el proceso de difusión cada
molécula individual se mueve en línea recta hasta que choca con algo -otra
molécula o la pared del recipiente- y luego rebota y sigue otra dirección. Las moléculas
continúan moviéndose aunque se hayan distribuido uniformemente por un espacio dado;
sin embargo, con la misma rapidez conque algunas moléculas se mueven, por ejemplo,
de izquierda a derecha y otras se mueven de derecha a izquierda, de modo que se
mantiene un equilibrio. Cualquier número de substancias se difundirán independientemente
unas de otras en la misma solución, aunque la difusión sea rápida en distancias cortas,
una molécula necesita mucho tiempo para recorrer distancias de unos cuantos centímetros.
Existen varios tipos de difusión:
-
Diálisis: Es el paso de una sustancia disuelta por una
membrana dotada de permeabilidad diferencial. Si se llena con solución de azúcar
una bolsa de colodión, celofán o pergamino, y se sumerge en un vaso de agua, las
moléculas de azúcar dializan por la membrana ( si los poros son lo bastante grandes).
-
Osmosis: Se define como la difusión de agua o moléculas
de solvente a través de una membrana.
En resumen: La diálisis es la difusión de partículas
disueltas (soluto) a través de una membrana semipermeable, y la ósmosis es
la difusión de las moléculas de solventes a través de la misma.
MATERIAL,
SUSTANCIAS y REACTIVOS:
|
MATERIAL: |
SUSTANCIAS y REACTIVOS: |
|
Un vaso de precipitados de 300 mililitros. |
Agua. |
|
Una probeta de 250 mililitros. |
Azúcar. |
|
Una cinta métrica. |
Un huevo. |
|
Una balanza analítica. |
Ácido acético (CH3COOH) |
METODOLOGÍA:
· Se preparó una solución de ácido acético al 15%, posteriormente se tomaron las mediciones de la circunferencia
longitudinal y transversal del huevo, así como su masa original. Se sumergió
el huevo en 200 ml de ácido acético al 15% y se dejó reposar durante la noche.
Se realizaron mediciones de la circunferencia (longitudinal y transversal)
y masa al siguiente día, así como el volumen final del fluido en el vaso.
· Terminando
lo anterior, se colocó el mismo huevo en 200 ml de una solución de glucosa
al 20.27%. Se dejó reposar durante toda la noche, al día siguiente se realizaron
las mediciones de circunferencias, masa del huevo y medida del volumen final
del fluido en el vaso.
· Agua
(destilada): terminado lo anterior, el mismo huevo se introdujo en 200ml de
agua. se dejó reposar durante una noche. Se midió la masa, la circunferencia
del huevo y el volumen final del fluido en el vaso.
|
|
Masa
|
Circunferencia Longitudinal
|
Circunferencia Transversal
|
Fluido Inicial
|
Fluido Final
|
|
Huevo Natural
|
67.15g
|
16.8cm
|
15.0cm
|
|
|
|
Ácido Acético
|
75.97g
|
17.5cm
|
15.5cm
|
200ml
|
175ml
|
|
Glucosa
|
74.67g antes
82.75g después
|
18.0cm
|
16.5
|
200ml
|
193ml
|
|
Agua Destilada
|
92.71g
|
18.7cm
|
16.9
|
200ml
|
190ml
|
|
Concentración de Glucosa (Molaridad)
|
Masa Inicial (gramos)
|
Masa Final (gramos)
|
Cambios
de la masa (%)
|
|
0.0
|
25.1
|
26.3
|
4.78
|
|
0.2
|
25.9
|
28.4
|
9.65
|
|
0.4
|
26.1
|
30.0
|
14.94
|
|
0.6
|
26.3
|
30.1
|
14.45
|
|
0.8
|
25.9
|
30.6
|
18.15
|
|
1.0
|
30.7
|
37.6
|
22.48
|
En el laboratorio nosotros examinamos el
proceso de difusión a través de la membrana semipermeable de un huevo, algo similar
es lo que ocurre en células vivas.
Nosotros primero colocamos el huevo en ácido
acético. El ácido acético fue necesario para disolver el cascaron y exponer la membrana,
el cascarón comenzó a burbujear a medida de que se disolvió, transcurrido un considerable
lapso de tiempo (24 horas), el cascaron se disolvió completamente, permitiendo que
se difunda el agua (contenida en la solución de ácido acético al 30%) hacia el huevo.
Podemos de cierta forma afirmar esta aseveración dado que el volumen del huevo
aumentó y esto se verificó midiendo el fluido final. Y por último podemos afirmar
que muy probablemente una pequeña pizca de ácido también penetró la membrana ya
que terminado el experimento, al romperse la membrana, el huevo despedía cierto
olor al ácido acético.
Al colocar el huevo en la solución de glucosa,
el agua de esta solución, atravesó la membrana y se difundió por ella hacia
el interior del mismo. Muy probablemente la glucosa tuvo una larga difusión a través
de la membrana debido al aumento del volumen del sistema.
Cuando colocamos el huevo en el agua destilada. El sistema permitió difundir más agua a través de la membrana hacia
dentro de el huevo. Por lo
tanto el huevo
aumentó su volumen
y por consecuencia se incrementaron las circunferencias
longitudinal y transversal, dando por resultado que el
volumen de agua en
el vaso disminuyera.
En el primer experimento (solución
de ácido acético), después de colocar el huevo dentro de esta solución este
comenzó a burbujear. Con esto comprobamos que existe una reacción entre el ácido
acético y el carbonato de calcio de la cáscara del huevo, todo esto está sustentado
por el hecho de que la cáscara estuvo completamente consumida a la mañana siguiente.
Con esto pudimos comprobar que efectivamente se realizo el proceso de ósmosis
por el hecho de que el experimento nos arrojo una variación de masa y volumen en
el huevo, así como la disminución de fluido en el vaso de precipitados que lo contenía.
En el segundo experimento (solución
de glucosa), no se cumplió con el objetivo, por que teóricamente el volumen y la
masa del huevo tienden a disminuir y el volumen de fluido final en el vaso de precipitados
tiende a aumentar. En relación a lo anterior en nuestros resultados obtuvimos un
aumento de masa y volumen del huevo y una disminución en el volumen del fluido
en el vaso de precipitados.
Para mejorar esta fase del experimento se
recomienda lo siguiente:
·
Cuando se saque el huevo
de la solución de ácido acético ( para realizar las mediciones respectivas), es
necesario tener ya preparada la solución de glucosa para que nuestro sistema no
sufra alteraciones debidas al medio ambiente.
·
Cuando se efectúen las
mediciones respectivas se cada fase del experimento hay que tomar en cuenta que
se deben de seguir ciertas reglas como son: utilizar guantes para no llenar de impurezas
los objetos que estamos manejando. También debemos de vigilar rigurosamente
la limpieza del equipo que estamos utilizando. Todo esto lo hacemos a mención de
que para obtener resultados más precisos debemos seguir reglas, y estas
nos ayudaran a cometer errores lo menos posible.
En el tercer experimento (agua destilada), nuestro objetivo
se cumplió dado que se esperaba un aumento de volumen y masa,
bastante considerable (con respecto a las dos experimentaciones anteriores),
y una disminución de volumen de fluido en el vaso de precipitados.
Para mejorar esta fase del experimento se recomienda lo siguiente:
Comenzar el experimento
de difusión y osmosis en día lunes o martes, por el tiempo que
se requiere para llevarse a cabo.
-
Claude A. Ville, Biología, Séptima edición, Editorial
Interamericana, México 1985. Pág. 34 a la 43.
-
Ralph H. Petrucci, Química General, Fondo Educativo
Interamericano, E. U. A. 1977. Pág. 183 a la 185.
-
Samuel H. Maron y Carl F. Prutton, Fundamentos de
Fisicoquímica, Décima edición, editorial Limusa, México 1979. Pág.
25.
|