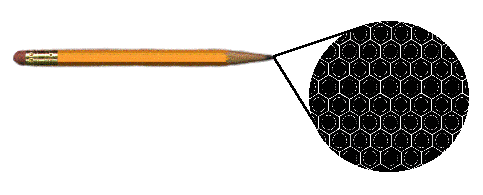
El carbono es
un elemento curioso. Se presenta en formas y colores diversos. Quizá
los más comunes son sólidos negros (coke, grafito) pero también
se puede presentar como el cristalino y duro diamante. Efectivamente, los
diamantes están pura y simplemente formados por átomos de
carbono. Claro está que en los diamantes esos átomos de carbono
están ordenados de una forma muy especial, que sólo se consigue
bajo presiones muy altas. Así que en este caso esas piedras tan
preciosas son escasas y caras no debido a su composición sino
a las extrañas condiciones bajo las que se forman.
En cualquier
caso el garfito es un material muy común y barato que se puede encontrar
en las minas de los lápices. Los cristales de diamante son tan escasos
y difíciles de extraer que llegamos a pagar el equivalente de muchos,
muchos, muchos lápices para conseguir uno y usarlo en rituales de
apareamiento.
En el grafito
los átomos de carbono forman capas en las que cada átomo
está rodeado por otros tres átomos idénticos a él
formando una estructura hexagonal. En el diamante cada átomo de
carbono está enlazado a cuatro vecinos iguales dispuestos en forma
de tetrahedro.

La estructura
de cada uno de estos dos materiales, es decir, el orden interno de sus
átomos, es lo que determina sus propiedades. El enlace en tres dimensiones
de los átomos de carbono en el diamante da lugar a una estructura
más robusta y por tanto a cristales más duros que en el caso
del grafito. En este último el enlace se limita a las dos dimensiones
de las capas, que pueden deslizarse fácilmente entre sí lo
cual da lugar a un material blando que se usa como lubricante sólido.
Todo esto se
sabe desde hace ya muchos años. Pero hace poco el carbono irrumpió
con fuerza de nuevo en el mundo de los materiales gracias a una aparición
estelar con nuevas ropas. En 1985 se descubrió una nueva forma del
carbono (de hecho una familia entera de nuevas formas). El primer miembro
de esta familia y el mejor conocido es una forma con estructura esférica,
compuesta por 60 átomos de carbono, y que se muestra en la
siguiente figura:

Esta bola de fórmula C60 se conoce también como "buckminsterfullerene" o simplemente "fulereno" en honor del ingeniero americano R. Buckminster Fuller. Fuller había diseñado, ya en 1967, para la EXPO en Montreal, una cúpula geodésica en la que usaba elementos hexagonales junto con alguno pentagonal para curvar la superficie. La molécula de fulereno es verdaderamente un asombroso conjunto de 60 átomos de carbono (esferas azules en el dibujo de arriba), todos ellos equivalentes, indistinguibles, cada uno enlazado a otros tres carbonos, como en el grafito, pero con una topología peculiar, formando parte de dos hexágonos y un pentágono que da lugar a una estructura cerrada.
Esta nueva forma
del carbono se puede aislar a partir del hollín que se produce al
hacer saltar un arco eléctrico entre dos electrodos de grafito.
Algo así como un experimento de relámpagos a escala de laboratorio.
Es QUÍMICA A ALTAS TEMPERATURAS que da lugar a MOLÉCULAS
CALENTITAS !.
Otros fulerenos y
materiales similares han seguido al C60 en los titulares, entre ellos el
C70, una molécula con forma de balón de football americano,
también estructuras de capas concéntricas como las cebollas
y nanotubos cilíndricos (tubos de dimensiones en nanometros, es
decir 0.000000001 metros). La historia de los fulerenos es un ejemplo perfecto
de un extraordinario nuevo producto químico, fruto de una excelente
investigación básica, que ha dado lugar a un nuevo campo
de la investigación química y al desarrollo de nuevos materiales
que encontrarán sin duda numerosas aplicaciones en toda clase de
dispositivos de alta tecnología.
Y ¿qué
decir de su curiosa forma? . Bueno... podemos asegurar que Buckminster
Fuller no fue la única persona capaz de combinar sabiamente hexágonos
y pentágonos para formar una esfera. Algún otro humano anónimo
ya tuvo la misma idea porque el C60 es ¡ exactamente
idéntico a un balón de fútbol !

Última modificación: 9 Feb
1999
©Pedro Gómez-Romero, 1998, 1999
![]() De vuelta a la página principal sobre Ciencia, Tecnología
y Sociedad
De vuelta a la página principal sobre Ciencia, Tecnología
y Sociedad