- Σύμφωνα με τη θεωρία των κρούσεων μία κρούση μεταξύ των μορίων των αντιδρώντων οδηγεί στη δημιουργία των προϊόντων
- πάντοτε
- μόνο αν τα μόρια των αντιδρώντων έχουν κατάλληλο προσανατολισμό
- μόνο αν τα αντιδρώντα έχουν μία ελάχιστη κινητική ενέργεια
- αν τα μόρια των αντιδρώντων έχουν κατάλληλο προσανατολισμό και μία ελάχιστη κινητική ενέργεια
- Το παρακάτω ενεργειακό διάγραμμα αναφέρεται στην αντίδραση Α → Β όταν πραγματοποιείται υπό σταθερή πίεση. Από το διάγραμμα προκύπτει ότι η ενθαλπία (ΔΗ) και η ενέργεια ενεργοποίησης (Ea) της αντίδρασης είναι αντίστοιχα
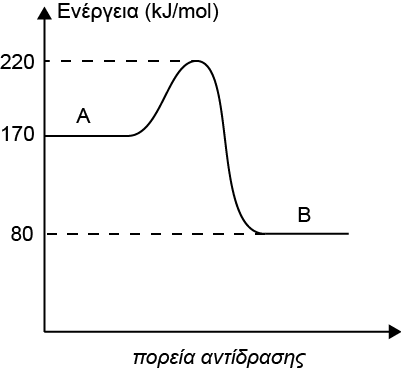
- +220 kJ/mol και 90 KJ/mol
- -90 kJ/mol και 50 KJ/mol
- -90 kJ/mol και 140 KJ/mol
- -140 kJ/mol και 50 KJ/mol
- Σε ένα δοχείο πραγματοποιείται η αντίδραση: 2Ν₂ + 3Ο₂ → 2Ν₂Ο₃
Αν σ’ ένα χρονικό διάστημα ο μέσος ρυθμός μεταβολής , κατ’ απόλυτη τιμή, της συγκέντρωσης του Ο₂ είναι 0,6 Μ/s τότε στο ίδιο χρονικό διάστημα ο μέσος ρυθμός μεταβολής της συγκέντρωσης του Ν₂Ο₃ είναι:- 0,6 M/s
- 0,4 M/s
- 0,3 M/s
- 0,2 M/s
- Σε δοχείο πραγματοποιείται η αντίδραση μεταξύ αερίων: Α + 2Β → 2Γ. Στο παρακάτω διάγραμμα παριστάνεται η μεταβολή της συγκέντρωσης δύο αερίων της αντίδρασης. Τότε:
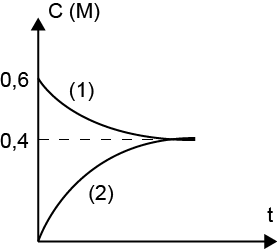
- η (1) αντιστοιχεί στο Α και η (2) στο Β
- η (1) αντιστοιχεί στο Α και η (2) στο Γ
- η (1) αντιστοιχεί στο Β και η (2) στο Γ
- Μία αντίδραση ολοκληρώνεται σε 8 min και παράγονται 2 mol ενός προϊόντος Α.
Τότε, στη γενική περίπτωση, τη στιγμή 4 min- θα έχει παραχθεί ποσότητα 1 mol A
- θα έχει παραχθεί ποσότητα μικρότερη από 1 mol A
- θα έχει παραχθεί ποσότητα μεγαλύτερη από 1 mol A
- Η μέση ταχύτητα της αντίδρασης 2Α(g) + B(s) → Γ(g) + 2Δ(g) υπολογίζεται από τη σχέση:
-
- Στη γενική περίπτωση για την αντίδραση Α → Β η μέση ταχύτητα της αντίδρασης από 0 – t₁
- είναι ίση με τη στιγμιαία ταχύτητα τη στιγμή t₁
- είναι μεγαλύτερη από τη στιγμιαία ταχύτητα τη στιγμή t₁
- είναι μικρότερη από τη στιγμιαία ταχύτητα τη στιγμή t₁
- Το ενεργοποιημένο σύμπλοκο
- έχει μεγαλύτερη ενέργεια από τα αντιδρώντα σε κάθε αντίδραση
- έχει μεγαλύτερη ενέργεια από τα αντιδρώντα μόνο στις ενδόθερμες αντιδράσεις
- έχει μεγαλύτερη ενέργεια από τα αντιδρώντα μόνο στις εξώθερμες αντιδράσεις
- έχει μικρότερη ενέργεια από τα αντιδρώντα σε κάθε αντίδραση
- Η ενέργεια ενεργοποίησης μιας αντίδρασης μεταβάλλεται όταν
- μεταβληθεί η θερμοκρασία
- μεταβληθούν οι αρχικές συγκεντρώσεις των αντιδρώντων
- προστεθεί καταλύτης
- μεταβληθεί η πίεση
- Σε υδατικό διάλυμα HCl προστίθεται ένα έλασμα Zn οπότε πραγματοποιείται η αντίδραση:
Zn(s) + 2HCl(aq) → ZnCl₂ (aq) + H₂(g). ν πριν την προσθήκη του Zn προσθέσουμε στο διάλυμα του HCl μικρή ποσότητα στερεού ΚΟΗ τότε η αρχική ταχύτητα της αντίδρασης- θα αυξηθεί
- θα ελαττωθεί
- δεν θα μεταβληθεί
- Θεωρούμε ότι η αύξηση της θερμοκρασίας κατά 10° C διπλασιάζει την ταχύτητα μιας αντίδρασης.
Αν μία αντίδραση στους 50° C έχει αρχική ταχύτητα υ, τότε στους 80° C και για τις ίδιες αρχικές ποσότητες των αντιδρώντων θα έχει αρχική ταχύτητα ίση με:- 3υ
- 4υ
- 8υ
- 30υ
- Σε δοχείο όγκου V εισάγονται ποσότητες C και CO₂ οπότε πραγματοποιείται η αντίδραση
C + CO₂ → 2CO. Ποια από τις παρακάτω μεταβολές ελαττώνει την αρχική ταχύτητα της αντίδρασης;- οι ίδιες ποσότητες αντιδρώντων εισάγονται στο ίδιο δοχείο αλλά σε μεγαλύτερη θερμοκρασία
αλλά ο C βρίσκεται με τη μορφή μικρότερων κόκκων - οι ίδιες αρχικές ποσότητες αντιδρώντων εισάγονται στο ίδιο δοχείο και στην ίδια θερμοκρασία
- οι ίδιες ποσότητες αντιδρώντων εισάγονται σε δοχείο όγκου 2V στην ίδια θερμοκρασία
- διπλάσιες ποσότητες αντιδρώντων εισάγονται στο ίδιο δοχείο στην ίδια θερμοκρασία
- οι ίδιες ποσότητες αντιδρώντων εισάγονται στο ίδιο δοχείο αλλά σε μεγαλύτερη θερμοκρασία
- Η καταλυτική προσθήκη υδρογόνου στο αιθένιο
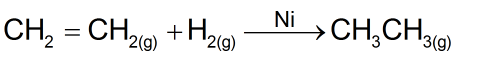
- είναι παράδειγμα ομογενούς κατάλυσης και ερμηνεύεται με τη θεωρία της προσρόφησης
- είναι παράδειγμα ομογενούς κατάλυσης και ερμηνεύεται με τη θεωρία των ενδιαμέσων προϊόντων
- είναι παράδειγμα ετερογενούς κατάλυσης και ερμηνεύεται με τη θεωρία της προσρόφησης
- είναι παράδειγμα ετερογενούς κατάλυσης και ερμηνεύεται με τη θεωρία των ενδιαμέσων προϊόντων
- Ο κύριος λόγος για τον οποίο η ταχύτητα μιας αντίδρασης αυξάνεται σημαντικά με μικρή αύξηση της θερμοκρασίας είναι ότι
- ελαττώνεται η ενέργεια ενεργοποίησης
- αυξάνεται σημαντικά ο συνολικός αριθμός των κρούσεων
- αυξάνεται σημαντικά ο αριθμός των μορίων που έχουν ενέργεια μεγαλύτερη από την ενέργεια ενεργοποίησης
- Από τα παρακάτω διαγράμματα ποιο παριστάνει τη μεταβολή της ταχύτητας μιας ενζυμικά καταλυόμενης αντίδρασης σε συνάρτηση με τη θερμοκρασία;
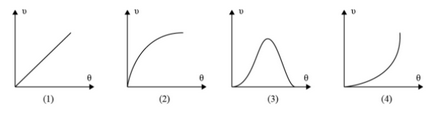
- το (1)
- το (2)
- το (3)
- το (4)
- Σε υδατικό διάλυμα οξαλικού οξέος (COOH)₂ προσθέτουμε με σταθερό ρυθμό όξινο διάλυμα KMnO₄. H ταχύτητα της αντίδρασης που πραγματοποιείται
- συνεχώς ελαττώνεται
- συνεχώς αυξάνεται
- αρχικά ελαττώνεται από κάποια στιγμή και μετά αυξάνεται και τελικά ελαττώνεται ξανά
- είναι συνεχώς σταθερή
- Ποια από τις παρακάτω προτάσεις που αφορούν τα ένζυμα είναι λανθασμένη
- έχουν απόλυτη εξειδίκευση
- έχουν μεγάλες σχετικές μοριακές μάζες
- είναι πιο αποτελεσματικά από τους μη βιοχημικούς καταλύτες
- η δράση τους δεν επηρεάζεται από το pH του διαλύματος
- Σε κλειστό δοχείου όγκου V εισάγονται ποσότητες από τα αέρια Α και Β και σε σταθερή θερμοκρασία πραγματοποιείται η αντίδραση: A(g) + B(g) → Γ(g).
H πίεση στο δοχείο:- είναι σταθερή σε όλη τη διάρκεια της αντίδρασης
- ελαττώνεται συνεχώς μέχρι να ολοκληρωθεί η αντίδραση
- αυξάνεται συνεχώς μέχρι να ολοκληρωθεί η αντίδραση
- αρχικά αυξάνεται και από ένα σημείο και μέχρι την ολοκλήρωση της αντίδρασης ελαττώνεται
- Σε μία αντίδραση η διαφορά της ενθαλπίας μεταξύ αντιδρώντων και προϊόντων ισούται με το ποσό θερμότητας που εκλύεται ή απορροφάται από την αντίδραση αυτή
- πάντα
- όταν η αντίδραση πραγματοποιείται υπό σταθερή πίεση
- όταν η αντίδραση πραγματοποιείται υπό σταθερή θερμοκρασία
- όταν η αντίδραση πραγματοποιείται υπό σταθερό όγκο
- Κατά την πλήρη καύση των υδρογονανθράκων η ενθαλπία των προϊόντων είναι
- πάντα μεγαλύτερη από την ενθαλπία των αντιδρώντων
- πάντα μικρότερη από την ενθαλπία των αντιδρώντων
- πάντα ίση με την ενθαλπία των αντιδρώντων
- κάποιες φορές μεγαλύτερη και κάποιες άλλες φορές μικρότερη από την ενθαλπία των αντιδρώντων