|
Descubridor
(es): Prehistoria
Elemento
químico de símbolo Zn, número atómico 30 y peso atómico 65.37. Es un metal
maleable, dúctil y de color gris. Se conocen 15 isótopos, cinco de los cuales
son estables y tienen masas atómicas de 64, 66, 67, 68 y 70. Cerca de la mitad
del zinc común se encuentra como isótopo de masa atómica 64.
Los usos más
importantes del zinc los constituyen las aleaciones y el recubrimiento protector
de otros metales. El hierro o el acero recubiertos con zinc se denominan
galvanizados, y esto puede hacerse por inmersión del artículo en zinc fundido
(proceso de hot-dip), depositando zinc electrolíticamente sobre el artículo como
un baño chapeado (electrogalvanizado), exponiendo el artículo a zinc en polvo
cerca de su punto de fusión (sherardizing) o rociándolo con zinc fundido
(metalizado).
El zinc es uno
de los elementos menos comunes; se estima que forma parte de la corteza
terrestre en un 0.0005-0.02%. Ocupa el lugar 25 en orden de abundancia entre los
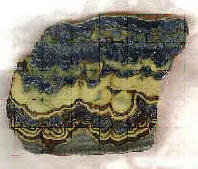
elementos. Su principal mineral es la blenda, marmatita o esfalerita de zinc,
ZnS. Es un elemento esencial para el desarrollo de muchas clases de organismos
vegetales y animales. La deficiencia de zinc en la dieta humana deteriora el
crecimiento y la madurez y produce también anemia. La insulina es una proteína
que contiene zinc. El zinc está presente en la mayor parte de los alimentos,
especialmente en los que son ricos en proteínas. En promedio, el cuerpo humano
contiene cerca de dos gramos de zinc.
El zinc puro y
recientemente pulido es de color blanco azuloso, lustroso y moderadamente duro
(2.5 en la escala de Mohs). El aire húmedo provoca su empañamiento superficial,
haciendo que tenga color gris. El zinc puro es dúctil y maleable pudiéndose
enrollar y tensar, pero cantidades pequeñas de otros metales como contaminantes
pueden volverlo quebradizo. Se funde a 420ºC (788ºF) y hierve a 907ºC (1665ºF).
Su densidad es 7.13 veces mayor que la del agua, ya que un pie cúbico (0.028m3)
pesa 445 Ib (200 Kg).
El zinc es
buen conductor del calor y la electricidad. Como conductor del calor, tiene una
cuarta parte de la eficiencia de la plata. A 0.91ºK es un superconductor
eléctrico. El zinc puro no es ferromagnético.
Es un metal
químicamente activo. Puede encenderse con alguna dificultad produciendo una
flama azul verdosa en el aire y liberando óxido de zinc en forma de humo. El
zinc metálico en soluciones ácidas reacciona liberando hidrógeno para formar
iones zinc, Zn2+. Se disuelve también en soluciones fuertemente
alcalinas para formar iones dinegativos de tetrahidroxozincatos, Zn(OH)2-4,
escrito algunas veces como ZnO2-2.en las fórmulas de los
zincatos.
El zinc es
siempre divalente en sus compuestos, excepto algunos cuando se une a otros
metales, que se denominan aleaciones de zinc. Forma también muchos compuestos de
coordinación. En la mayor parte de ellos la unidad estructural fundamental es un
ion central de zinc, rodeado por cuatro grupos coordinados dispuestos
espacialmente en las esquinas de un tetraedro regular.
|