
A.Transformation ou réaction ?
La France a décidé qu'à partir de la fin de la seconde, il fallait différencier la transformation chimique de la réaction chimique.
La réaction chimique est associée à la transformation. L’équation chimique symbolise la réaction chimique.
B. Les outils liés à la réaction chimique
Utilisation de la simple flèche 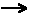
 |
Après l'introduction de la notion d’équilibre chimique, fini de jouer aux Indiens pour représenter comme avant, par une flèche, la réaction chimique en fin de seconde, en première et en terminale . |
Utilisation du signe =
 |
À partir de maintenant, l’utilisation du
signe égal pour symboliser la réaction
chimique est préconisée, même dans le
cas de transformation totale. Si cette écriture ne
présume pas du sens dans lequel se fera la
transformation (la réaction n’est pas
orientée), il est important de remarquer
qu’il vaut mieux écrire
l’équation chimique dans le sens où
la transformation se produit. |
Utilisation de la double flèche ![]()
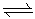 |
L'utilisation de la double flèche est exclusivement réservée à la représentation de mécanismes réactionnels. |
L’avancement x, exprimé en mol, décrit
l’évolution du système au cours de la
transformation. Il faut donc dire avancement de la
réaction.
Avec l’introduction des équilibres chimiques, il est
nécessaire de distinguer dans les notations
l’avancement maximal xmax (avancement atteint
lors d’une transformation totale) et l’avancement
à l’état final xf
(avancement atteint lors d’une transformation
limitée).
Équation: aA + bB = cC + dD (A, B : réactifs ; C, D : produits )
x (mol) : avancement de la réaction
n(A)0 : quantité de matière initiale (mol) de A
n(A) : quantité de matière (mol) de A à la date t
n(A)f : quantité de matière finale (mol) de A
Tableau d'avancement ou tableau d'évolution de la réaction :
| Équation chimique | a A + b B = c C + d D | ||||
|
|
|
|
|||
| Initial |
|
|
|
|
|
| En cours | x |
|
|
|
|
| Final |
|
|
|
|
|
Attention de bien différencier le quotient de
réaction de la constante d’équilibre.
Pour une réaction d’équation chimique
a A + b B = c C + d D , on peut écrire dans un état z du système :
Qr,z= [D]zd. [C]zc/ [A]za. [B]zb
Dans cette définition [A], [B], [C] et [D] sont des
nombres sans dimension
égaux aux valeurs des concentrations volumiques molaires
effectives.
La contribution du solvant et des solides est égale
à 1 dans cette définition.
Le quotient de réaction n’est en aucune façon lié à la constante d’équilibre.
À l’équilibre seulement, on peut écrire Qr,éq = K.
Il est dangereux d’écrire : K = [D]éqd. [C]éqc/ [A]éqa. [B]éqb, mais il faut écrire Qr,éq =[D]éqd. [C]éqc/ [A]éqa. [B]éqb= K
La constante d’équilibre K est une donnée obtenue à partir des tables thermodynamiques. Elle est en effet rigoureusement définie et liée à l’enthalpie libre par :
K = exp(– DrG° / RT) DrG° : enthalpie libre R : constante des gaz parfaits T : température en KPour l'étudiant, c’est :
- Une donnée caractérisant la réaction à une température donnée ;
- Une valeur qu’il peut déterminer expérimentalement en mesurant les concentrations à l’équilibre et en calculant le quotient de réaction à l’équilibre.
- Pour les réactions acido-basiques, la constante d’équilibre s’exprime en fonction des constantes d’acidités des deux couples acide/base intervenant dans la réaction. Il est alors nécessaire de passer par l’écriture du quotient de réaction à l’équilibre.
À bannir : le terme de constante de réaction
Dorénavant, on parle de vitesse de réaction et
plus de vitesse d’apparition du produit ou de disparition
d’un réactif. La vitesse est définie en
fonction de l’avancement :
v = (1/V) dx/dt
Les notions de vitesse moyenne, vitesse d’apparition ou
de disparition ne sont plus définies. Pour comparer
l’évolution temporelle de deux transformations, il
faut :
- comparer les coefficients directeurs des tangentes aux courbes
x= f(t) ;
- comparer les temps de demi-réaction.
Pour déterminer si une transformation est totale ou limitée, il faut calculer le taux d’avancement final.
On ne parle plus de transformation peu avancée ou très avancée ou quasi-totale …. Il ne reste que les transformations dites totales et les transformations limitées conduisant à un état d’équilibre.
La transformation totale
On considère qu’une transformation est totale quand le taux d’avancement final de la réaction associée est proche de 1. Il est donc nécessaire d'être sensibilisé aux effets des erreurs de mesures sur le taux d’avancement final. Dans certains cas, on obtient des valeurs supérieures à 1.
À bannir absolument : la réaction est totale, c’est la transformation qui est totale.
La transformation limitée
Une transformation est limitée si le taux d’avancement final de la réaction est inférieur à 1.
État d’équilibre
Une transformation limitée conduit à un
état d’équilibre, où les
concentrations des produits et des réactifs
n’évoluent plus. C’est un état
dynamique, qui ne se traduit pas par l’absence de
réaction mais par la coexistence de deux réactions
inverses se produisant à la même vitesse au niveau
microscopique. Au niveau macroscopique aucune transformation
n’est observée. Tout système chimique
évolue spontanément vers l’état
d’équilibre.
Il faut écrire que le système atteint
l’état d’équilibre, et non que la
réaction est à l’équilibre ou la
réaction est équilibrée.
Le système évolue spontanément vers
l’état d’équilibre.
La comparaison de Qr et de K permet de prévoir
dans quel sens le système va évoluer.
- si Qr < K le système évolue dans le
sens d’écriture de l’équation
- si Qr = K on est à
l’équilibre
- si Qr > K le système évolue dans le
sens contraire d’écriture de
l’équation.
C.Transformations totales ou limitées, sens d’évolution du système
Pour déterminer si une transformation est totale ou limitée, il faut calculer le taux d’avancement final.
Dans ce programme on ne parle plus de transformation peu avancée ou très avancée ou quasi-totale …. Il ne reste que les transformations dites totales et les transformations limitées conduisant à un état d’équilibre.
La transformation totale
On considère qu’une transformation est totale quand le taux d’avancement final de la réaction associée est proche de 1. Il est nécessaire d'être sensibilisé aux effets des erreurs de mesures sur le taux d’avancement final. Dans certains cas, on obtient des valeurs supérieures à 1.
À bannir absolument : la réaction est totale, c’est la transformation qui est totale.
La transformation limitée
Une transformation est limitée si le taux d’avancement final de la réaction est inférieur à 1..
État d’équilibre
Une transformation limitée conduit à un
état d’équilibre, où les
concentrations des produits et des réactifs
n’évoluent plus. C’est un état
dynamique, qui ne se traduit pas par l’absence de
réaction mais par la coexistence de deux réactions
inverses se produisant à la même vitesse au niveau
microscopique. Au niveau macroscopique aucune transformation
n’est observée. Tout système chimique
évolue spontanément vers l’état
d’équilibre.
Il faut écrire que le système atteint
l’état d’équilibre, et non que la
réaction est à l’équilibre ou la
réaction est équilibrée.
Le système évolue spontanément vers
l’état d’équilibre.
La comparaison de Qr et de K permet de prévoir
dans quel sens le système va évoluer.
- si Qr < K le système évolue dans le
sens d’écriture de l’équation
- si Qr = K on est à
l’équilibre
- si Qr > K le système évolue dans le
sens contraire d’écriture de
l’équation.
D. Le titrage
Le dosage est un terme général qui décrit
la détermination d’une concentration molaire
volumique. Dans le cas d’un dosage par ajout d’une
solution titrante avec repérage de
l’équivalence, on parle de titrage. Par opposition,
on réalise un dosage spectrophotométrique.
À chaque ajout de solution titrante le système
atteint un nouvel état. On peut décrire le dosage
de l’espèce A par la solution titrante B par le
tableau descriptif suivant :
| Equation chimique | a A + b B = c C + d D | ||||
| État du système | Avancement | Quantité de matière (mol) | |||
| Initial | x=0 | cA.VA | cB.VB,versé | 0 | 0 |
| En cours | x | cA.VA - a.x | cB.VB,versé – b.x | c.x | d.x |
Les quantités de matière initiales correspondent
aux quantités des réactifs versées à
un instant donné du titrage.
L’équivalence est définie comme étant
le changement de réactif limitant, les quantités de
réactifs sont alors nulles.
À l’équivalence, le volume de solution B versée est VE etles quantités de réactifs introduits sont nulles, on a donc ;
cA.VA- a.x = 0 cB.VE – b.x = 0 De la première équation on tire xéq : xéq = cA.VA/a
On introduit xéq dans la deuxième équation : cB.VE – (b.cA.VA)/a = 0 d’où cA = cB.( a.VE /b.VA).
On ne parle plus de dosage en retour, mais de titrage
indirect.
Pour les titrages indirects, la solution la plus simple consiste
à construire deux tableaux descriptifs liés. Il
faut alors prendre soin de différencier les notations des
avancements des deux réactions.
À une solution contenant l’espèce à
titrer A, on ajoute un excès de solution contenant
l’espèce titrante B. L’excès de B est
ensuite dosé par une espèce C.
Les tableaux descriptifs traduisant l’évolution du
système sont :
| Equation chimique | a A + b = c C | |||
| État du système | Avancement | Quantités de matières | ||
|
Initial |
x = 0 | cA.VA | cB.VB | 0 |
| Final | xf | cA.VA –a.xf =0 | cB.VB –b.xf | c.xf |
|
Équation chimique |
b’ B + d’ D = e’ E |
|||
|
État |
Avancement |
Quantités de matières |
||
|
Initial |
x’ = 0 |
cB.VB–b.xf |
cD.VD,versé |
0 |
|
Équivalence |
x’E |
cBVB–b.xf –b’.x’E |
cD.VD,versé–d’.x’E |
e.x’E |
À l’équivalence du titrage de B par D, le
volume de solution D versée est VE, les
quantités de réactifs introduits sont nulles, on a
donc :
cD.VE– d’.x’E
= 0 permet de calculer
x’E
cB.VB–
b.xf–b’.x’E = 0 permet de
calculer xf
on en déduit alors
cA : cA =
a.xf/VA
Si la dénomination d’acide fort et d’acide faible disparaît, il est nécessaire de distinguer les acides (respectivement les bases) dont la transformation avec l’eau est totale des autres. En effet, la formule utilisée pour écrire l’équation de dosage en dépend. Soulignons que les étudiants ne sont pas sensés savoir quels sont les acides « forts » et « faibles ». Il faut donc le leur préciser, en disant que la transformation est totale ou en donnant le taux d’avancement de la réaction avec l’eau.