AL2(SO4)3. - Alcalinizantes: hidroxido de cálcio, e sódio, carbonato de sódio, para conferir a alcalinidade necessária para a coagulação, em algumas estações não é adicionado nenhum produto pois a alcalinidade natural da água já é suficiente para coagulação. - Coadjuvantes: polieletrólitos por exemplo, que é utilizado para melhorar a capacidade de floculação.
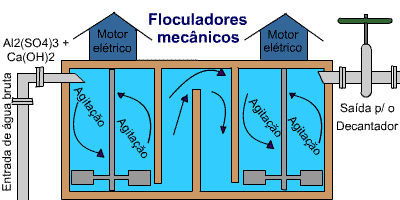 |
Baseado em "Operação e Manutenção de ETA" CETESB 1973