Caracterización de la respuesta
inmune hacia paramiosina en la cisticercosis humana y murina.
José Vázquez Talavera y Juan Pedro Laclette
I. RESUMEN
La paramiosina de la Taenia solium (TPmy) es un
antígeno inmunodominante en la cisticercosis humana y porcina; además, las
paramiosinas son candidatos a vacuna en contra de la esquistosomosis y la
filariasis. Hay pocos estudios para identificar las regiones de importancia
inmunológica de la paramiosina. En este estudio se encontraron diferencias en
el reconocimiento de tres regiones de la molécula, a pesar de que la TPmy es
una molécula fibrosa particularmente homogénea. Las células mononucleares de
sangre periférica de individuos sanos de un área endémica para cisticercosis
proliferaron con mayor proporción al ser estimuladas con el extremo amino y la
porción central de la TPmy. En contraste, las células de individuos con
neurocisticercosis proliferaron con la misma proporción contra cualquier
región. En otros experimentos se empleó a la TPmy para inducir protección en el
modelo murino. Los resultados indican que el extremo amino-terminal induce
alrededor del 60% de protección contra la infección por el cisticerco de Taenia
crassiceps. Esta protección se puede relacionar con una respuesta inmune
tipo Th1 y la proliferación de linfocitos T. Finalmente, al localizar los
epitopos de los linfocitos B los resultados mostraron que los anticuerpos de
humanos infectados naturalmente y los de ratones inmunizados con la TPmy
reconocieron, principalmente, el extremo carboxilo-terminal.
II. ABSTRACT
Taenia solium paramyosin (TPmy) is an immunodominant antigen in human
and porcine cysticercosis, paramyosins shown promise as a vaccine candidate
against schistosemiosis and some filariasis. There are few studies directed to
identify the immunologically relevant regions of paramyosin. In this work,
remarkable differences in the recognition of distinct regions of the molecule
were found, in spite of that TPmy is a particularly homogenous fibrous
molecule. Mononuclear cells of healthy individuals from an endemic area for
cysticercosis were more responsive towards the amino terminal end and the
central region of TPmy. In contrast, the responsiveness of cells from
neurocysticercotic patients showed no preference to any region of TPmy. A
second line of experiments involved protection studies using TPmy as vaccine in
the murine model. Results showed that the amino end induced about 60%
protection against a challenge with Taenia crassiceps cisticerci.
Protection seems to be related to a Th1-like immune response and to specific T
cell proliferation. Finally, characterization studies of B cell epitopes
indicated that antibodies in the sera of patients and TPmy-immunized mice
recognize predominantly epitopes located in the carboxyl-terminal fragment.
III. PRÓLOGO
La
cisticercosis es un problema de salud pública que afecta la economía en algunos
países de Latinoamérica, Asia y África. Esta enfermedad es causada por el
establecimiento del cisticerco de Taenia
solium en los tejidos del hombre y del cerdo. Actualmente, no se cuenta con
alguna vacuna establecida que prevenga la enfermedad en humanos o cerdos. Se ha
propuesto a las paramiosinas (proteínas del músculo de invertebrados) como
antígenos candidatos para el desarrollo de una vacuna en contra de la
esquistosomosis y la filariasis, que son también parasitosis provocadas por helmintos.
En nuestro laboratorio se ha clonado y expresado el gen de la paramiosina de la
T. solium (TPmy), así como de
diferentes fragmentos de éste. En el modelo murino de cisticercosis hemos
demostrado que la vacunación con fragmentos de la TPmy puede inducir niveles de
protección que alcanzan un 70%, en promedio. En el presente proyecto,
pretendemos comprender cuál es el tipo de respuesta inmune generada contra la
TPmy, para establecer estrategias en un eventual empleo de la TPmy contra la
cisticercosis porcina.
En
la primera publicación (Apéndice 1) que incluye la presente tesis “Human T- and
B-cell epitope mapping of Taenia solium Paramyosin” por los autores José
Vázquez-Talavera, Carlos F. Solís, Edith Medina-Escutia, Zoila Morales-López,
Jefferson Proaño, Dolores Correa, and Juan P. Laclette, se describe que los
anticuerpos de los pacientes con neurocisticercosis reaccionan principalmente
con la región carboxilo-terminal y reaccionan escasamente con la región
amino-terminal. En contraste, la respuesta inmune celular no mostró preferencia
por alguna región de la TPmy, si bien los individuos sanos respondedores lo
hicieron preferentemente contra la región amino-terminal.
En la segunda
publicación (Apéndice 2) “Characterization and Protective Potential of the
Immune Response to Taenia solium
Paramyosin in a Murine Model of Cysticercosis.” Por los autores José Vázquez-Talavera, Carlos F.
Solís, Luis I. Terrazas, and Juan P. Laclette, se concluye que la inmunización
con TPmy recombinante induce protección parcial contra un reto subsecuente con
el cisticerco de T. crassiceps y que esta capacidad protectora reside
básicamente en el tercio amino-terminal. Además, que la respuesta inmune contra
este tercio tiene un fenotipo Th1.
Y en la tercera
publicación (Apéndice 3) “Cellular immune response and Th1/Th2
cytokines in human neurocysticercosis: lack of immune supresión” por los
autores Edith Medina-Escutia, Zoila Morales-López, Jefferson V. Proaño, José
Vázquez, Victor Bermúdez, Vianney Ortiz-Navarrete, Vicente Madrid-Marina,
Juan P. Laclette and Dolores Correa. Se describe que los pacientes con
neurocisticercosis no muestran las evidencias de inmunosupresión que se
observan en los modelos animales.
1.
Ciclo de vida
El ciclo
de vida de T. solium se puede dividir en dos etapas; la primera ocurre
en el hospedero intermediario y la segunda en el definitivo (Figura 1).
El ser humano es el único hospedero definitivo del gusano adulto y es el
responsable de la infección de los hospederos intermediarios humano y porcino.
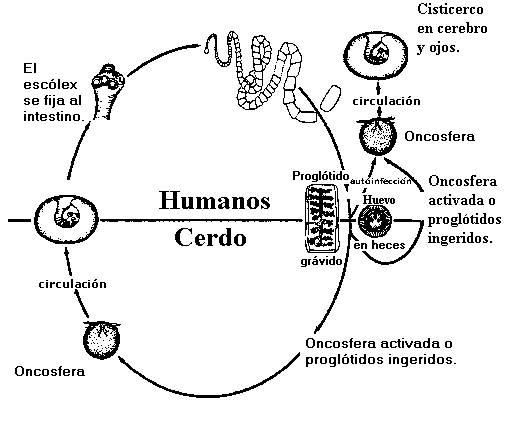
Figura
1. Ciclo de vida de la Taenia solium.
(Tomado con modificaciones de: http://www.dpd.cdc.gov/dpdx/HTML/Taeniasis.htm).
Desarrollo en el hospedero intermediario. La primera etapa se inicia con la
ingestión de los huevos de T. solium (Figura 2) por el
hospedero intermediario. Las enzimas proteolíticas del estómago e intestino
destruyen al embrióforo (una de las envolturas protectoras que protegen al embrión
para sobrevivir en el medio ambiente)
liberando al embrión (44[L1], 102[L2]). Se cree que el embrión hexacanto activado (también conocido como
oncosfera) atraviesa la mucosa intestinal por la acción combinada de sus
ganchos (31[L3]) que desgarran el tejido y de secreciones líticas que
digieren la mucosa. Posteriormente, el embrión alcanza los capilares sanguíneos
y linfáticos que lo llevan a diferentes órganos, en donde se desarrolla hasta
convertirse en un cisticerco.
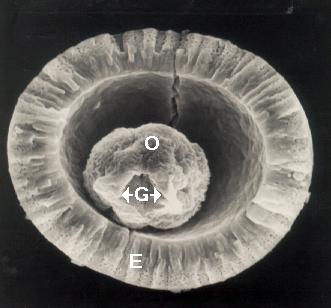
Figura 2. Micrografía
electrónica de barrido de un huevo de Taenia
solium. E: embrioforo, G: ganchos oncosferales, O: oncosfera (Tomada de 44[L4]).
El cisticerco (Figura 3) es una vesícula translúcida, ovoide o circular de 5 a
10 mm de diámetro con un pequeño gusano o escólex metido hacia dentro
(invaginado), que puede permanecer en los tejidos del hospedero intermediario
durante varios años (19[L5], 20[L6]), rodeado por una cápsula de tejido conectivo. La
vesícula está llena de un fluido
transparente que contiene proteínas del parásito y del huésped (6[L7]). Cabe hacer notar que el tegumento y la pared
vesicular (Figura 4) son el sitio de contacto del parásito
con el hospedero y desempeña un papel central en el mantenimiento de la
relación hospedero-parásito.
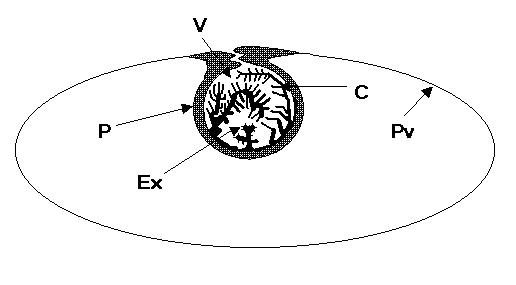
Figura
3. Ilustración esquemática de la larva o cisticerco de Taenia solium. C: canal espiral, Ex: escólex, P: pared vestibular,
Pv: pared vesicular y V: espacio vestibular.
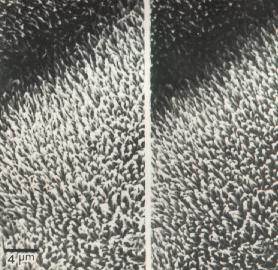
Figura
4. Superficie externa de la pared vesicular
de un cisticerco de Taenia solium en la cual se pueden distinguir las
microtricas (Tomada de 82[L8]).
Desarrollo
del cisticerco en el hospedero definitivo:
El ciclo de vida continúa cuando el ser humano
consume carne de cerdo infectada e ingiere uno o varios cisticercos viables. La
masticación, las sales biliares y las proteasas digestivas destruyen la pared vesicular e inducen la
salida o evaginación del escólex (9[L9]).
Una vez evaginado, el escólex (Figura 5) se fija en la pared
del yeyuno por medio de sus ventosas y ganchos rostelares (9[L10]).
A partir de entonces el escólex comienza a crecer y diferenciarse
hasta convertirse en gusano adulto.
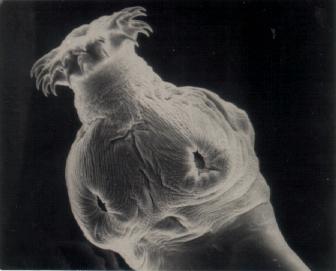
Figura
5. Micrografía electrónica de barrido del escólex de un cisticerco evaginado de
Taenia solium (cortesía del Dr. Juan Pedro Laclette).
La tenia adulta
mide entre 1.5 m y 5 m de longitud y su cuerpo esta formado por el escólex, el
cuello y el estróbilo. El estróbilo es una cadena de segmentos o proglótidos
que se desarrollan a partir del cuello. Los proglótidos poseen cientos de
testículos y un ovario trilobulado (Figura 6), por lo que se
piensa que se autofecunda para producir hasta 50,000 huevos infectantes (4[L11]). La contaminación de aguas y alimentos con los huevos
es favorecida por el fecalismo al aire libre, el hacinamiento y la falta de
higiene personal. Se ha
demostrado que el principal factor de riesgo es la presencia de un portador de
tenia en el ambiente cercano (18[L12],
89[L13],
90[L14],
91[L15],
92[L16],
93[L17]).
El ciclo de vida se cierra cuando el
hospedero intermediario ingiere los huevos que contaminan alimentos y agua.
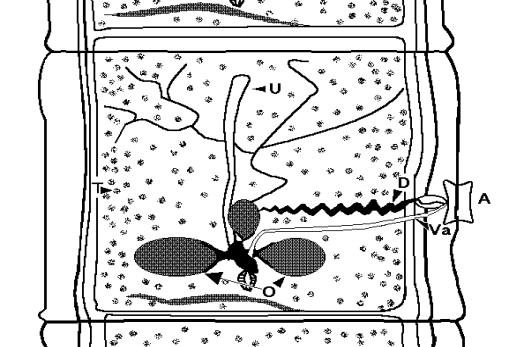
Figura 6.
Representación esquemática de un proglótido de Taenia solium, enfatizando al aparato reproductor. A: atrio
genital, D: ducto genital, O: ovario trilobulado, T: testículos, U: útero y Va:
vagina.
2. Importancia de la cisticercosis
La
cisticercosis humana es un problema de salud pública en México y otros países (24[L18], 26[L19]). En un estudio realizado en 1982, se calculan pérdidas
económicas anuales equivalentes a 350 millones de dólares americanos, debidas a
la incapacidad laboral de individuos con cisticercosis (115[L20]). La curación de enfermos con neurocisticercosis tiene
un costo de 21 mil millones de pesos al año (88[L21]). También, se ha calculado que, durante 1986, el costo
del cuidado médico de 2,700 nuevos casos de neurocisticercosis ascendió a 14.5
millones de dólares americanos; además, el 75% de los individuos adquieren la
cisticercosis en edad productiva (24[L22]). En 1984, el gobierno de México estableció como
prioritario un programa de salud para el control y la eradicación
epidemiológicos (24[L23]).
En
cuanto a la cisticercosis porcina, existen diversos estudios que han tratado de
estimar la prevalencia de ésta, en diferentes regiones del país. El estudio más
completo es el realizado con los registros de 75 rastros en 22 estados de la
República, el cuál se puede ver en la tabla I (3[L24]).
Tabla I. Prevalencia de la cisticercosis en diferentes
regiones de país (Tomada de 3[L25]).
|
Localidad |
Frecuencia |
Año |
|
|
Aguascalientes |
Aguascalientes |
0.52 |
1980 |
|
Chihuahua |
Chihuahua Chihuahua Chihuahua |
0.49 3.32 1.65 |
1980 1980 1981 |
|
Colima |
Varios |
2.40 |
1980 |
|
Coahuila |
Torreón |
2.37 |
1981 |
|
Distrito Federal |
Ciudad de México |
0.16 |
1981 |
|
Durango |
Durango |
2.21 |
1980 |
|
Guanajuato |
Ocampo San Felipe |
10.0 3.0 |
1981 1981 |
|
Jalisco |
Guadalajara |
0.005 |
1981 |
|
Michoacán |
La Piedad |
10.0 |
1980 |
|
Morelos |
Varios Cuernavaca |
1.9 0.37 |
1980 1980 |
|
Nuevo León |
Monterrey |
0.016 |
1981 |
|
Querétaro |
Querétaro |
0.74 |
1981 |
|
Sonora |
Hermosillo |
0.07 |
1980 |
|
Tamaulipas |
Ciudad Victoria |
0.37 |
1980 |
|
Tlaxcala |
Huamantla Apizaco |
0.63 3.30 |
1980 1980 |
|
Veracruz |
Jalapa Veracruz Tuxpan |
0.11 0.75 1.08 |
1980 1980 1980 |
|
Yucatán |
Mérida |
0.04 |
1980 |
|
Zacatecas |
Jerez Fresnillo Zacatecas |
0.75 2.10 1.26 |
1980 1980 1980 |
|
Tabasco |
No se encontró información |
||
|
Campeche |
|||
La
cisticercosis porcina causa considerables pérdidas económicas. En 1980 más de
43 millones de dólares se perdieron por decomisos de los rastros (2[L26]). Cabe mencionar que la
cisticercosis porcina es susceptible al tratamiento con drogas cestocidas (24[L27]).
Se
puede decir que la cisticercosis es un problema de salud pública que se
mantiene por ignorancia, y falta de recursos (24[L28]). La costumbre de dejar
deambular a los cerdos (Figura 7)
incrementa el riesgo de que adquieran la cisticercosis por ingerir heces humanas contaminadas con huevos de T. solium. Los animales cisticercosos
detectados en la inspección post-mortem
deben ser decomisados y procesados adecuadamente para evitar destruir la carne.
Cuando el animal infectado llega a un rastro, los animales cisticercosos son
decomisados; sin embargo, en nuestro país, algunos animales infectados son
distribuidos clandestinamente y no pasan la inspección veterinaria.

Figura 7. El cerdo es el hospedero intermediario de Taenia solium.
4.
Inmunología de la cisticercosis humana y porcina
La
presencia de los cisticercos en los tejidos de su hospedero humano o porcino
induce la formación de una respuesta inmune. La respuesta inmune humoral del
hospedero cisticercoso ha sido estudiada principalmente de una manera indirecta
en trabajos relacionados con el inmunodiagnóstico. Se ha encontrado que la
respuesta humoral no participa con la destrucción del metacéstodo. Los humanos
con cisticercosis tienen anticuerpos contra el cisticerco y, a pesar de ello,
el parásito sobrevive por periodos relativamente prolongados. Algunos estudios
han mostrado que el tiempo promedio para la aparición de los síntomas después
de la infección en los pacientes es de 7 años y puede llegar hasta los 20 años
(20[L29])
La IgG es
la inmunoglobulina predominante entre los anticuerpos anti-cisticerco, en
humanos (14[L30], 28[L31]). Inicialmente se mostró que los sueros de pacientes
reconocen por inmunoelectroforesis hasta 8 antígenos y por Western blot más de
20 (27[L32]). En la cisticercosis humana los cisticercos presentan
abundante IgG del hospedero asociada a la superficie, sin embargo, estas
moléculas tampoco se relacionan con el daño en los cisticercos (14[L33]). También, se ha informado que hay anticuerpos humanos
contra el glicocálix, componentes del citoplasma de los citones tegumentales,
antígenos del estroma y del sistema ductural, pero no se ha encontrado en
contra del tegumento del canal espiral, ni del músculo de las ventosas del escólex
(100[L34]). En la cisticercosis porcina, la superficie del
cisticerco, así como la cápsula inflamatoria formada por el hospedero, están
cubiertas por inmunoglobulinas del cerdo (99[L35]). También, se ha descrito una molécula de 55 kDa que se
une a la región Fc de las inmunoglobulinas (57[L36]).
Además,
el hospedero es capaz de producir un infiltrado inflamatorio, cuyo perfil
molecular es complejo y puede eventualmente eliminar al parásito. Por ejemplo,
en el humano, en la cisticercosis meníngea, una de las formas relativamente
benignas de la enfermedad, la reacción inflamatoria, es en general, escasa y el
infiltrado está compuesto por linfocitos, células plasmáticas y epitelioides,
pocas veces células gigantes y rara vez se observan eosinófilos. En contraste,
en el caso de la cisticercosis meníngea cisternal, una de las formas más
graves, la reacción inflamatoria está constituida por numerosas células
inflamatorias entre las que se identifican linfocitos, células plasmáticas,
algunos cuerpos de Russell, células epitelioides, numerosas células gigantes,
pocos son polimorfonucleares y eosinófilos (80[L37]). El caso de la respuesta del cerdo es diferente. En la cisticercosis porcina en músculo esquelético, los eventos
celulares durante la destrucción del parásito sugieren un proceso secuencial
comenzado por los eosinófilos. Una vez iniciada la destrucción, se incrementan
los macrófagos, células epitelioides, así como células gigantes que invaden la
cavidad para fagocitar el exudado y los restos de la larva. Los linfocitos
forman agregados similares a folículos, simultáneamente los eosinófilos parecen
retirarse de la región más interna del proceso inflamatorio y se observan
dispersos entre los demás elementos de la reacción granulomatosa (5[L38]). Cabe señalar que un punto
discordante radica en el tipo de infiltrado celular de la cisticercosis humana
y de la porcina, ya que en el padecimiento humano casi no hay eosinófilos, lo
cual ha sido explicado por el hecho de que la eosinofilia es un fenómeno
temprano.
Las
personas infectadas pudieran tener mayor susceptibilidad a otras enfermedades,
lo cuál puede sugerir cierta inmunodeficiencia (14[L39]). Se ha descrito que la
proliferación celular a mitógenos se encuentra disminuida en pacientes con
cisticercosis (14[L40]), pero la evidencia es
contradictoria (99[L41], Apéndice 3). La disminución de la
proliferación celular también ha sido descrita en la cisticercosis porcina (34[L42], 65[L43], 68[L44], 106[L45]). Incluso se ha informado un factor de RNA que inhibe la
activación de linfocitos por fitohemaglutinina (67[L46]). Sin embargo, se ha encontrado que los extractos del
metacéstodo de la T. solium pueden ser mitogénicos para
linfocitos de ratón (99[L47]).
Es consistente el hecho
de que la disminución de la proliferación
celular ha sido descrita en la cisticercosis murina por T. crassiceps (96[L48], 116[L49]) y por T. taeniaeformis (50[L50]). Respecto a esto se ha reportado que antígenos
de excreción/ secreción del cisticerco de T. crassiceps pueden inhibir
la proliferación de linfocitos T (103[L51]).
Se ha propuesto que el cisticerco
emplea varios mecanismos para evadir la respuesta inmune del hospedero y
sobrevivir por largos periodos (14[L52]). Entre los mecanismos propuestos se
pueden mencionar: 1) secreción de antígenos inmunodominantes para desviar a los
anticuerpos lejos de la superficie ("cortina de humo"), 2)
enmascaramiento de la superficie con moléculas del hospedero, 3) modulación o
supresión de la respuesta inmune del hospedero, 4) establecimiento del parásito
en hospederos inmunosuprimidos y 5) alojamiento en lugares inmunológicamente
privilegiados, como el sistema nervioso (14[L53]).
Se ha
desarrollado un modelo de cisticercosis intraocular en conejos, la evidencia
obtenida en este modelo indica que el cisticerco se puede establecer en sitios
inmunológicamente privilegiados, pero que una vez que el hospedero se ha
presensibilizado, los parásitos no se desarrollan (10[L54]).
5. Vacunación
contra la cisticercosis
Se
puede inducir inmunidad en cerdos con antígenos de excreción/ secreción
obtenidos en cultivos de oncosferas (75[L55]),
con extractos antigénicos del cisticerco de T.
solium (65[L56],
73[L57])
o de T. crassiceps (58[L58],
95[L59]).
También se puede proteger ratones de la infección por T. solium y T. saginata
con antígenos oncosferales de estos parásitos (66[L60]).
En el caso de la T. ovis y de la T. taeniaeformis, se ha demostrado una
alta protección utilizando proteínas oncosferales de excreción/ secreción o sus
formas recombinantes (38[L61],
39[L62]).
Las formas recombinantes empleadas en el caso de T. ovis, también,
inducen una elevada protección en la cisticercosis porcina (78[L63]).
También se han detectado antígenos totales de T. crassiceps que pueden correlacionarse con la respuesta inmune protectora. (95[L64]). Recientemente, se han publicado revisiones
sobre la vacunación contra la cistcercosis (25[L65], 55[L66]).
En el desarrollo de
vacunas contra los céstodos ténidos se han empleado oncosferas vivas con
resultados muy positivos; se ha logrado inducir protección homóloga contra T. ovis, T.hydatigena y E. granulosus
en borrego y T. pisiformis en
conejos; la protección es más efectiva si el embrión eclosiona; además, se
puede inducir inmunidad con oncosferas irradiadas para limitar la migración o
colonización a otros tejidos (83[L67]). También, se ha logrado inducir protección con
extractos completos de oncosferas contra T.
saginata, T. hydatigena, T. ovis y T. taeniaeformis (83[L68]). Se ha demostrado que se puede inducir protección
contra H. nana y se puede lograr
protección contra el establecimiento/ supervivencia/ fecundidad de gusanos de E. granulosos en perros. Se ha sugerido
que la infección previa de perros con gusanos de E. granulosus puede inducir protección, así como la inmunización
oral con protoescólices irradiados, antígenos obtenidos de protoescolices o
membranas de cisticercos. También, se puede inducir cierta protección contra E. granulosus con la inmunización
parenteral de oncosferas activadas de E.
granulosus, T. hydatigena, T. ovis, T. multiceps, T. pisiformis y T.
serialis (54[L69]).
Por otro lado, se ha
demostrado que los antígenos liberados por oncosferas vivas son capaces de
proteger contra T. ovis, T. taeniaeformis, T. hydatigena, T. pisiformis
y T. saginata (83[L70]). Una sola inmunización con antígenos del cultivo de
oncosfera de T. ovis emulsificados en
adyuvante incompleto de Freund inducen inmunidad protectora que dura 12 meses
en ovejas. Sin embargo, lo mismo no se ha logrado con ganado y se piensa que la
permanencia del antígeno tiene un papel determinante; incluso, se ha publicado que
en corderos existen niveles elevados de anticuerpos protectores con una vida
media corta contra T. ovis y T. hydatigena y, aparentemente, ocurre
algo similar en la infección del conejo con T.
pisiformis. Esto sugiere que en ausencia del antígeno, el anticuerpo
protector tiende a desaparecer (83[L71]).
El desarrollo de una vacuna útil para
el control de la taeniasis/ cisticercosis no es simple. Al respecto, se ha
informado que la vacunación con altas dosis de antígeno de T. crassiceps en cerdos (95[L72])
y en ratón (98[L73])
parecen no ser protectoras o incluso podrían facilitar la infección, mientras
que bajas dosis inducen la reducción de la carga parasitaria; también, se ha
sugerido que el adyuvante empleado podría alterar la eficiencia de la
protección en cerdos (95[L74]).
Asimismo, se ha propuesto que algunos anticuerpos podrían facilitar la
infección de T. solium en cerdos (95[L75])
y de T. crassiceps en ratón (94[L76])
y se ha encontrado que el genotipo puede influenciar la respuesta inmune a la
infección por T. crassiceps en
ratón (97[L77])
y lo mismo se ha sugerido en la cisticercosis porcina (95[L78]).
6. Mecanismo
inmunológico humoral de protección
Los estudios sobre el mecanismo inmune
de protección se han realizado principalmente en modelos experimentales de rata
y ratón. En estos modelos se ha encontrado que el mecanismo de protección
dependerá de la etapa de desarrollo del parásito. En rata y ratón se ha visto
que la resistencia natural a la infección por oncosferas de T. taeniaeformis tiene componentes humorales.
Esta resistencia se detecta en suero a partir de la segunda semana de
infección. Existe evidencia que el mecanismo de resistencia depende del
complemento. Sin embargo, después de la primera semana se pierde parte de la
susceptibilidad del parásito a este mecanismo humoral de ataque. No obstante,
después de esta etapa es posible inducir resistencia con extractos de
cisticercos; la resistencia, si bien es humoral, depende de un perfil de
isotipos diferente al producido después de la infección oral. Por otra parte,
la IgA se ha involucrado en la resistencia natural pasiva transferida de ratas
madres a sus crías durante la lactancia (117[L79]).
En ovejas se ha
encontrado que la inmunidad inducida con antígenos liberados por cisticercos en
cultivo se puede transferir de la madre a las crías por el calostro (83[L80]). En la hidatidosis ovina, la inmunidad no se
transfiere pasivamente de madre a hijo (54[L81]).
La
vacunación con antígenos de oncosferas de T.
taeniaeformis ocasionan que muy pocas o ningún metacéstodo se establezcan,
sin embargo las que llegan a establecerse permanecen viables y se desarrollan
normalmente. La vacunación con antígenos de metacéstodos permite la detección
de muchos parásitos después de las primeras semanas del reto; sin embargo, 5
semanas después son eliminados todos los parásitos; 60 días después se
evidencia que las lesiones remanentes de los parásitos eliminados desaparecen
gradualmente y muy pocas pueden detectarse macroscópicamente (53[L82]).
Estudios morfológicos en
oncosferas de H. nana que han
penetrado el epitelio intestinal de ratones inmunes sugieren que el daño de los
anticuerpos se localiza en la membrana externa del parásito. Además se ha
demostrado que los anticuerpos y el complemento son los principales mecanismos
que eliminan a las oncosferas. Sin embargo, la sensibilidad a este mecanismo se
pierde en cuanto las oncosferas comienzan con el desarrollo de
microvellosidades (83[L83])
También, ratones con
infección intraperitoneal primaria y ratones que no fueron protegidos por la
infección subcutánea de T. crassiceps
tuvieron niveles elevados de IgM, IgG1 y IgG3 séricos respecto a ratones
controles y los ratones protegidos. Se ha demostrado IgG2b e IgG3 en la
superficie de larvas viables de T.
crassiceps (32[L84]).
7. Mecanismo inmunológico celular de protección
Los eosinófilos han sido frecuentemente
relacionados con la destrucción del parásito. Este es el caso de la
cisticercosis porcina. En la infección natural del cerdo por el cisticerco de T. solium, los eventos celulares durante
la destrucción del parásito sugieren un proceso secuencial iniciado por los
eosinófilos (5[L85]).
Similarmente, en cerdos inmunizados con extractos de cisticerco de T. solium se han descrito varios tipos
celulares en el proceso inflamatorio que destruye al parásito, tales como:
eosinófilos, monocitos, linfocitos, macrófagos y células epitelioides. Sin
embargo, los eosinófilos son los que participan en la destrucción del
cisticerco, pues se ha encontrado que la inmunización induce eosinofilia. Estas
células forman la capa más interna de la reacción granulomatosa que rodea al
cisticerco, degranulan en las cercanías del parásito, se infiltran en el
tegumento y rodean a los restos del parásito destruido (63[L86],
64[L87],
65[L88],
73[L89]).
En el modelo murino de cisticercosis por T.
taeniaeformis se ha encontrado que después de que las oncosferas llegan al
hígado, aparentemente, los eosinófilos se convierten en elementos prominentes
de la respuesta inflamatoria que rodea y elimina las oncosferas (117[L90]).
En infecciones
intraperitoneales por T. crassiceps
las células del hospedero tienden a acumularse alrededor del polo que gema
antes de que se lleve a cabo la encapsulación del resto del cisticerco (32[L91]).
Además, al
inducir protección con antígenos homólogos de oncosfera, a la infección
intravenosa de huevos de T. solium o T. saginatus, se observa que los
ratones controles en los estudios histopatológicos muestran una reacción
inflamatoria alrededor del metacéstodo y en ocasiones bastante intensa, en
dónde se hallan macrófagos, linfocitos y células plasmáticas. Esta respuesta
inflamatoria es diferente de la documentada en esquistosomosis o en cerdos
infectados por T. solium, donde los
eosinófilos se encuentran en contacto con la superficie del parásito. Esto
puede sugerir que los eosinófilos no son atraídos hacia las etapas tempranas de
los metacéstodos, sino más bien son reclutados en contra de etapas más tardías
como en su hospedero natural (66[L92]).
Finalmente,
en la infección intraperitoneal de ratones con metacéstodos de T. crassiceps, la resistencia se ha
relacionado más claramente con la inmunidad celular que con anticuerpos (8[L93]).
8. Inmunología de la cisticercosis murina
El
empleo del modelo murino ha permitido el conocimiento de puntos críticos de la
inmunidad contra la cisticercosis, el modelo de cisticercosis murina por el
cisticerco de T. crassiceps se discutirá más adelante. La penetración
del epitelio intestinal y la diferenciación postoncosferal inmediata, son
fenómenos muy importantes en términos de la infección y la respuesta al reto en
animales inmunes; porque son en esos momentos cuando se inicia el contacto
entre los determinantes antigénicos y el sistema inmune del hospedero. En la
infección, el resultado es el desarrollo de una resistencia altamente
específica y efectiva contra un reto; sin embargo, el metacéstodo logra
establecerse e induce resistencia a infecciones similares posteriores. A partir
de 3-4 días después de la infección se observa la infiltración de células
fagocíticas atraídas probablemente por las células destruidas durante la
penetración del parásito y la aparición de eosinófilos en las triadas portales
(117[L94]).
Diferentes
modelos han proporcionado diferentes conclusiones. Por ejemplo, el mecanismo de
protección contra T. taeniaeformis en
ratones parece no depender de la participación de linfocitos T, ya que ratones
atímicos desnudos pueden ser protegidos de la infección por el parásito tan
sólo con suero inmune. Por otro lado, se ha publicado que poblaciones
enriquecidas de linfocitos B y T pueden causar reducción significativa de la
carga parasitaria, en menos tiempo del esperado para el mecanismo humoral (7[L95],
117[L96]).
Además, se ha informado que los cisticercos de T. taeniaeformis pueden sobrevivir por periodos largos en la
cavidad peritoneal de ratas tratadas con grandes dosis de suero inmune
protector (117[L97]).
8a. Inmunidad contra
el cisticerco de Taenia crassiceps
En el modelo murino experimental de cisticercosis por
el metacéstodo de T. crassiceps, el cisticerco se multiplica
asexualmente por gemación en la cavidad peritoneal del ratón (29[L98]). El metacéstodo se mantiene por medio de pases
sucesivos de ratón en ratón de tal manera que en este modelo experimental el
parasito no llega al estado adulto. Sin embargo, este modelo ha permitido
sugerir candidatos a vacuna contra la cisticercosis porcina (36[L99], 58[L100], 95[L101]).
Se puede inducir un
nivel elevado de resistencia a la reinfección con T. crassiceps por la inoculación subcutánea de cisticercos vivos de
T. crassiceps tres semanas antes del
reto (32[L102] ).
Incluso, se han identificado antígenos de cisticercos de T. crassiceps con la capacidad de inducir protección en cerdos (58[L103] ).
En la infección por T. crassiceps, se ha encontrado una
relación entre eosinofilia y resistencia a la infección: la esinofilia fue más
pronunciada cuando los cisticercos inyectados intraperitonealmente fueron
destruidos o controlados por el hospedero; y mientras más rápido se desarrolla
la eosinofilia, más eficiente es el control de los cisticercos (31[L104] ).
La inmunización
subcutánea con productos secretados-excretados de cisticercos de T. crassiceps en cultivo, con adyuvante completo
de Freund o alumbre, son tan efectivas para inducir protección como los
metacéstodos contra los cisticercos de T. crassiceps (32[L105] ).
Se
ha encontrado similitud antigénica entre T.
solium y T. crassiceps. Esta
similitud se puede aprovechar para inducir protección heteróloga. El suero de cerdos protegidos se ha usado para
identificar cuatro clonas de una biblioteca de cDNA de cisticercos de T. crassiceps con la capacidad de
inducir protección (58[L106] ).
Recientemente, se ha
sugerido que la respuesta Th1 ejerce control en la infección por el cisticerco
de T. crassiceps (108[L107] ,
116[L108] ). Se ha encontrado que la respuesta
protectora inducida con la inmunización con DNA está mediada por linfocitos T
productores de IL-2 e IFN-g (16[L109] ). Un péptido con capacidad de inducir
protección, también puede inducir la producción de IFN-g
(111[L110] ). De manera similar la administración in
vivo de IFN-g o anti-IL-10 reduce la carga parasitaria (109).
Se ha sugerido que la eliminación del parásito depende de una respuesta Th1
(IL-2 e IFN-g) (87[L111] ). En el laboratorio del Dr. Laclette
hemos obtenido resultados similares a estos (Apéndice 2). Además se ha
publicado que en esta infección se desarrolla una respuesta inmune mixta, es
decir, Th1 y Th2 (103[L112] , 110[L113] ). Previamente, en esquistosomosis, se ha
sugerido que la protección inducida por la paramiosina tiene un mecanismo tipo
Th1 (ver adelante).
9. La paramiosina de la
Taenia solium
 Uno de los antígenos mejor
caracterizados del cisticerco de la T.
solium es sin duda el antígeno B (AgB). Este antígeno fue caracterizado
inicialmente como un arco de precipitación sin carga neta aparente,
identificado por inmunoelectroforesis al confrontar un extracto de cisticercos
contra sueros de pacientes con neurocisticercosis (Figura 8).
En esta prueba, fue el antígeno reconocido con mayor frecuencia por anticuerpos
en sueros de pacientes con neurocisticercosis, es decir, se trata de un
antígeno inmunodominante (21[L114] , 119[L115] ).
Uno de los antígenos mejor
caracterizados del cisticerco de la T.
solium es sin duda el antígeno B (AgB). Este antígeno fue caracterizado
inicialmente como un arco de precipitación sin carga neta aparente,
identificado por inmunoelectroforesis al confrontar un extracto de cisticercos
contra sueros de pacientes con neurocisticercosis (Figura 8).
En esta prueba, fue el antígeno reconocido con mayor frecuencia por anticuerpos
en sueros de pacientes con neurocisticercosis, es decir, se trata de un
antígeno inmunodominante (21[L114] , 119[L115] ).
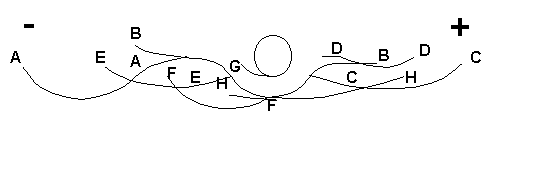
Figura 8. Diagrama
clásico de las 8 bandas de precipitación reconocidas por anticuerpos en sueros
humanos, enfrentados contra un extracto de cisticercos de Taenia solium,
mediante la técnica de inmunoelectrofofesis (Tomado de 26[L116] , 27[L117] ).
En 1982 se publicó el primer
método de purificación del AgB. Este método era complejo y laborioso y permitía
la purificación de pequeñas cantidades de proteína. El AgB purificado por el
método original mostraba dos bandas de 85 y 95 kDa en electroforesis en gel de
poliacrilamida (33[L118] ).
Accidentalmente
se encontró que el AgB se une a la colágena (79[L119] ),
lo que dio la pauta para desarrollar un procedimiento de purificación por
afinidad (Figura 9). El uso de este nuevo método de
purificación permitió mostrar que el péptido de 85 kDa era en realidad un
producto proteolítico de 95 kDa (41[L120] ).
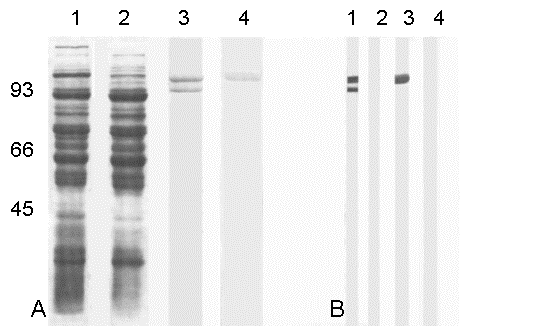
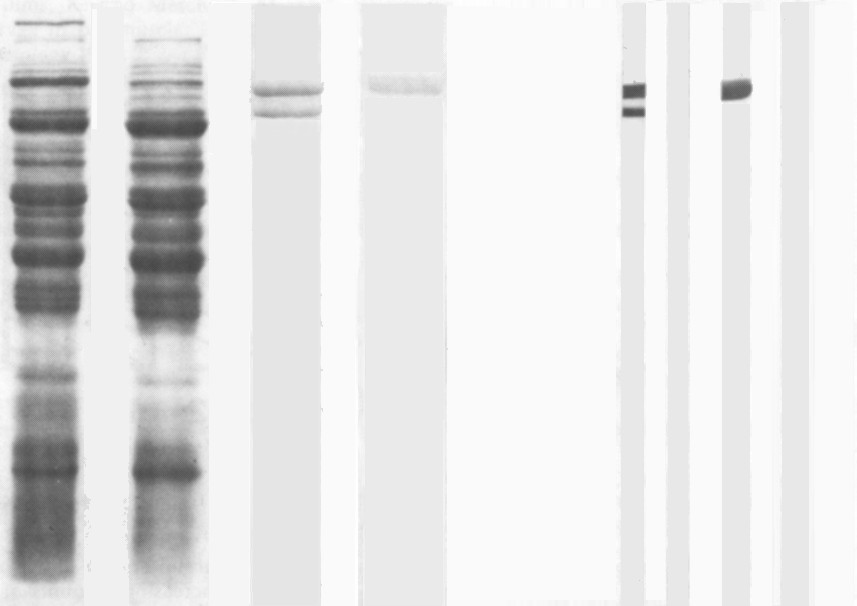
Figura 9. Purificación
del AgB de Taenia solium a partir de un extracto crudo de cisticercos
por afinidad a colágena. A: Gel de poliacrilamida teñido con azul de
Coomassie de: 1) extracto crudo de cisticercos, 2) extracto crudo de
cisticercos después de incubación con colágena polimérica. Fracciones unidas a
la colágena cuando el extracto crudo se incubó en ausencia (3) o en presencia
(4) de inhibidores de proteinasa. B: Inmuelectroforesis de la fracción
A3 (carriles 1 y 2) y A4 (carriles 3 y 4) incubadas con IgG de conejo anti-AgB
(tiras 1 y 3) y con suero normal de conejo (tiras 2 y 4) (Tomado de 45[L121] ).
La
localización de AgB en el cisticerco ha sido llevada a cabo por métodos de
inmunofluorescencia e inmunoperoxidasa indirecta, así como por métodos de
yodación radioactiva de la superficie (43[L122] ).
El antígeno se encontró ampliamente distribuido en el tejido del cisticerco,
con una fluorescencia más intensa en los citones tegumentales (43[L123] ,
45[L124] )
(Figura 10). Dado que estas células participan activamente
en la producción de proteínas y glicoproteínas que se envían
al citoplasma distal (56[L125] , 112[L126] ), se propuso que el
AgB podría ser sintetizado en los citones tegumentales y enviado al tegumento
para su liberación hacia los tejidos del hospedero (43[L127] ). Los resultados de
experimentos con inmunoperoxidasa indirecta y yodinación radioactiva de
superficie, indicaron que el AgB no era una proteína de superficie por lo que
se propuso que se trataba de un producto de excreción-secreción del parásito (43[L128] , 45[L129] ). Además, se puede
colectar AgB en el sobrenadante de cultivo in
vitro de cisticercos (45[L130] ) y se le puede
detectar en el líquido cefaloraquídeo de pacientes con neurocisticercosis (14[L131] ). Cabe señalar que
recientemente se ha detallado la localización del AgB en el tegumento de helmintos (47[L132] ).
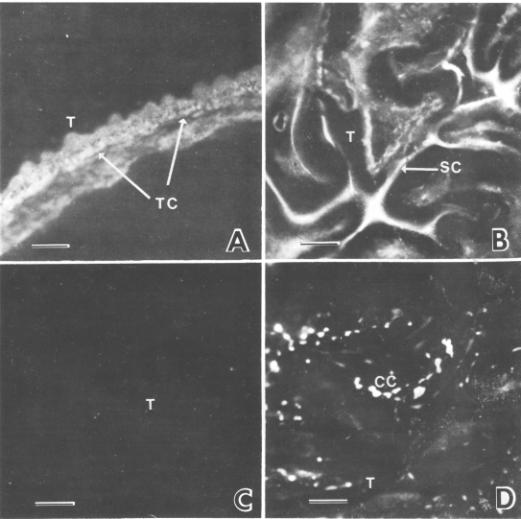
Figura 10.
Inmunofluorescencia indirecta de cortes del tegumento (A y C) y el escólex (B y
D) del cisticerco de Taenia solium incubado
con un suero anti-AgB (A y B) o suero de conejo normal (C y D). Cómo segundo
anticuerpo se usó un suero de chivo a-conejo
acoplado a isotiocianato de fluoresceína. C.C., corpúsculos calcáreos; S.C.,
canal espiral; T.C., citones tegumentales; T, tegumento. Barra=80 mm
(A y C), 90 mm (B y D) (Tomado de 43[L133] ).
La
posibilidad de que se trate de un producto de excreción-secreción concordaba
con su inmunodominancia y se correlacionaba bien con la producción intensa de
anticuerpos en las células plasmáticas que rodean al cisticerco en el músculo
de cerdo (17[L134] ).
Sin embargo no concuerda con el infiltrado inflamatorio débil en el granuloma que
rodea al cisticerco en el músculo esquelético del cerdo (5[L135] ).
La
relación entre el AgB y la reacción inflamatoria surgió a partir de su
propiedad de unión a colágena. Esto llevó ha cuestionar qué otras moléculas con
estructura colagénica podrían unirse al AgB. Entre las proteínas con estructura
colagénica cuya función se relaciona al sistema inmune, se encuentra el C1q.
Esta proteína es un subcomponente del C1, el primer componente de la cascada
del complemento.
Ensayos iniciales mostraron que
una preincubación de suero humano con AgB purificado, disminuye los niveles de
complemento funcional en el suero (45[L136] ).
La inhibición del C1, posiblemente debida a la unión del AgB con el C1q (Figura 11) (46[L137] ).
![]()

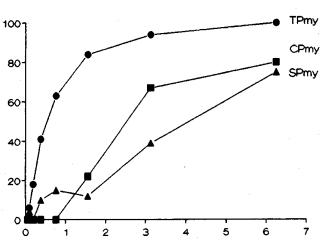
Figura 11.
Inhibición de la actividad del complemento por la paramiosina. Diferentes
cantidades de paramiosina se incubaron a 37°C por 30 min con C1 aislado. La
actividad residual de C1 se evaluó con un ensayo hemolítico (Tomado de 46[L138] ).
Una
secuencia parcial del AgB mostró homología con la secuencia también parcial de
la paramiosina del Schistosoma mansoni
(42[L139] ). A partir de este hallazgo fue posible
obtener clonas de cDNA que contienen la secuencia codificadora completa del AgB
de T. solium, tal como se muestra en
la figura 12 (49[L140] ). La secuencia de aminoácidos deducida a
partir de la secuencia nucleotídica codifica para una proteína de 863 residuos
de aminoácidos con un peso molecular de 98,000. El análisis de la secuencia de
aminoácidos mostró un 72% de similitud con la parmiosina de S. mansoni y alrededor de un 30% de
homología con paramiosinas de nemátodos como Caenorhabditis elegans y Dirophilaria
immitis o de artrópodos como
Drosophyla melanogaster (49[L141] ). También, se demostró identidad
inmunológica de la proteína recombinante, expresada en Escherichia coli, con el AgB (49[L142] ), además de identidad inmunológica
entre paramiosina de S. mansoni y el antígeno B. Estos resultados demuestran que el AgB es la
paramiosina de la T. solium (TPmy),
por lo que a partir de aquí se utilizará exclusivamente el término de
paramiosina. Las paramiosinas son proteínas del músculo de invertebrados (12[L143] , 43[L144] , 47[L145] ). La paramiosina es una proteína
filamentosa con estructura de un a-hélice
superenrollada que forma homodímeros paralelos (12[L146] ).
![]() TPmyX1
TPmyX1
1 ATGTCTGAATCACACGTCAAAATTTCTCGTACCATCATACGCGGGACTTCCCCAAGTACTGTTCGACTTGAGAGTCGCGTACGAGAACTGGAGGACCTGC
M S E S H
V K I S R T I
I R G T S
P S T V R L E
S R V R E
L E D L 33
101
TCGATCTTGAGCGAGATGCTCGCGTCCGGGCTGAACGCAATGCCAACGAGATGAGCATTCAGCTGGACACCATGGCTGAACGTCTTGACGAATTGAGTGG
L D L E R
D A R V R A E
R N A N E
M S I Q L D T
M A E R L
D E L S G 67
201
TACTTCCTCTCAGACTCACGATGCTATTCGCCGTAAGGATATGGAGATCTCGAAGCTGCGCAAGGATCTGGAAAATGCCAACGCTGCTTTCGAAACTGCC
T S S Q T
H D A I R R K
D M E I S
K L R K D L E
N A N A A
F E T A 100
301
GAGGCCACTCTGCGCCGCAAACACAACACCATGATCTCCGAGATCTCCAGCGAGGTTGAGAATTTGCAGAAGCAGAAGGGCAGGGCAGAGAAGGACAAGA
E A T L R
R K H N T M I
S E I S S
E V E N L Q K
Q K G R A
E K D K 133
401 GCCAGCTCATGCTTGAAATCGATAACGTTCTTGGTCAACTTGATGGCGCTTTAAAGGCCAAGGCCTCAGCGGAGAGCAAACTGGAGGGCTTGGACAGCCA
S Q L M L
E I D N V L G
Q L D G A
L K A K A S A
E S K L E
G L D S Q 167
501 GCTGACGCGCTTGAAGGCGCTGACCGACGATCTTCAACGCCAAATGGCCGACGCTAACTCTGCCAAGTCGCGTTTGGCCGCAGAGAACTTCGAATTGGTT
L T R L K
A L T D D L Q
R Q M A D
A N S A K S R
L A A E N
F E L V 200
601 CGCGTAAATCAGGAGTATGAAGCACAAGTCGTCACCTTCTCTAAGACAAAGGCCGCTCTTGAAAGCCAGCTGGATGACCTTAAACGGGCCATGGATGAAG
R V N Q E
Y E A Q V V T
F S K T K
A A L E S Q L
D D L K R
A M D E 233
![]() TPmyX6
TPmyX6
701
ATGCACGCAATCGCCTAAGCCTTCAAACACAGTTGTCGAGTCTGCAAATGGACTACGACAACCTGCAAGCACGTTACGAGGAGGAAGCCGAGGCAGCCGG
D A R N R
L S L Q T Q L
S S L Q M
D Y D N L Q A
R Y E E E
A E A A G 267
![]() TPmyX4
TPmyX4
801 AAATCTGCGCAACCAAGTTGCCAAATTCAACGCCGATATGGCTGCCCTCAAGACCCGTCTTGAGAGAGAACTTATGGCCAAGACTGAAGAGTTTGAAGAA
N L R N Q
V A K F N A D
M A A L K
T R L E R E L
M A K T E E F E
E 300
901
CTCAAACGCAAGCTGACTGTTCGCATTACCGAGTTGGAGGATATGGCTGAACATGAGCGCACTCGTGCCAACAACCTGGAGAAGACCAAAGTTAAGCTGA
L K R K L
T V R I T E L
E D M A E
H E R T R A N
N L E K T
K V K L 333
1001
CTCTTGAGATCAAGGATCTACAGGCTGAGAACGAGGCGTTGGCAGCAGAGAATGGAGAGTTAACGCATCGGGCGAACGAGGCAGAGAATCTTGCCAATGA
T L E I K
D L Q A E N E
A L A A E
N G E L T H R
A N E A E
N L A N E 367
1101 GCTGCAGCGTCGAATAGACGAGATGACAGTGGAAATCAACACCCTCAACTCGGCCAACAGCGCTCTAGAGGCGGACAACATGCGCCTCAAGGGGCAGGTC
L Q R R I
D E M T V E I
N T L N S
A N S A L E A
D N M R L
K G Q V 400
1201 GGTGACCTCACCGACCGCATCGCCAATCTCGACCGCGAAAACCGCCAACTTGGCGATCAACTGAAGGAGACGAAATCAGCCCTGCGTGATGCGAATCGTC
G D L T D
R I A N L D R
E N R Q L
G D Q L K E T
K S A L R
D A N R 433
1301 GACTGACCGATTTGGAGGCCCTGCGCAGTCAGTTGGAGGCAGAGCGTGACAACCTCGCCTCTGCTCTCCATGATGCTGAGGAGGCACTGAAGGAGATGGA
R L T D L
E A L R S Q L
E A E R D
N L A S A L H
D A E E A
L K E M E 467
1401 AGCGAAGTACGTTGCCTCGCAGAACGCTCTTAATCACCTCAAGTCCGAGATGGAACAACGTCTGCGTGAGAAGGACGAGGAACTGGAGAATCTGAGAAAG
A K Y V A
S Q N A L N H
L K S E M
E Q R L R E K
D E E L E
N L R K 500
1501 AGCACGACTCGCACGATTGAGGAGTTGACAACCACCATCTCAGAGATGGAGGTTCGCTTCAAGTCGGATATGTCTCGTCTGAAGAAGAAGTACGAGGCGA
S T T R T
I E E L T T T
I S E M E
V R F K S D M
S R L K K
K Y E A 533
![]()
![]() TPmyX7 TPmyX5
TPmyX7 TPmyX5
1601
CAATCAGCGAGCTAGAGGTGCAACTAGACGTGGCGAACAAGGCGAACGTCAACCTCAACCGCGAGAACAAAACCCTGGCTCAACGAGTTCAAGAGCTGCA
T I S E L
E V Q L D V A
N K A N V
N L N R E N K
T L A Q R
V Q E L Q 567
1701 GGCTGCGTTGGAGGACGAGCGACGAGCTCGCGAAGCTGCAGAGAGCAACTTGCAGGTGAGCGAGCGCAAACGCATCGCCCTTGCTTCGGAAGTGGAAGAG
A A L E D
E R R A R E A
A E S N L
Q V S E R K R
I A L A S
E V E E 600
1801 ATTCGCAGCCAACTGGAACTCAGTGACCGCGCTCGCAAGAACGCCGAGTCCGAACTCAACGATGCCAATGGACGTATCTCGGAGCTCACCCTATCGGTCA
I R S Q L
E L S D R A R
K N A E S
E L N D A N G
R I S E L
T L S V 633
1901 ACACTCTTACCAATGACAAACGTCGACTTGAAGGCGATATTGGCGTCATGCAGGGCGATCTCGATGAGGCCGTCAATGCGCGCAAGGCTGCTGAGGATAG
N T L T N
D K R R L E G
D I G V M
Q G D L D E A
V N A R K
A A E D R 667
2001
AGCTGACCGTCTGAACGCTGAGGTACTCCGCCTGGCTGATGAGCTGCGACAGGAACAAGAAAATTACAAGCGTGCTGAGACTCTGCGCAAGCAACTTGAG
A D R L N
A E V L R L A
D E L R Q
E Q E N Y K R
A E T L R
K Q L E 700
2101 ATCGAGATCCGTGAGATCACGGTCAAGTTGGAGGAGGCTGAGGCTTTCGCTACTCGTGAGGGTCGCCGTATGGTTCAAAAGCTCCAGAATCGGGTGAGGG
I E I R E
I T V K L E E
A E A F A
T R E G R R M
V Q K L Q
N R V R 733
2201 AGCTTGAGGCGGACGTGGACGGAGAAATTCGTCGCGCCAAGGAGGCCTTCGCCAACGCGCGCAAATACGAGCGTCAATTCAAGGAACTGCAGACACAGAG
E L E A D
V D G E I R R
A K E A F
A N A R K Y E
R Q F K E
L Q T Q S 767
2301 CGAGGATGATAAACGCATGATTTTGGAGCTTCAAGACCTGCTAGACAAGACTCAGATCAAGATGAAAGCCTACAAACGTCAGCTTGAGGAACAGGAAGAG
E D D K R
M I L E L Q D
L L D K T
Q I K M K A Y
K R Q L E
E Q E E 800
2401 GTGTCTCAGCTGACGATGAGCAAGTACCGTAAGGCGCAGCAACAGATTGAGGAGGCGGAACATCGTGCTGACATGGCGGAGAGGACGATCACCATTAAGA
V S Q L T
M S K Y R K A
Q Q Q I E
E A E H R A D
M A E R T
I T I K 833
![]() TPmyX2
TPmyX2
2501
GGACAATTGGTGGACCCGGTTCCCGCGCCGTTTCGGTGGTTCGGGAGATCAACAGTGTCTCCCGTGGTAACCGTGCAACCAGCATCATGTAGATGTCCTC
R T I G G
P G S R A V S
V V R E I
N S V S R G N
R A T S I
M - - - 863
Figura 12. Secuencia
nucleotídica y de aminoácidos de la región codificadora de la clona de cDNA de
la paramiosina de la Taenia solium.
Los codones de iniciación (ATG) y de terminación (TAG) se encuentran tachados.
Las secuencias subrayadas señalan las secuencias correspondientes a los
oligonucleótidos empleados para amplificar los fragmentos de la TPmy (Tomada de
49[L147] ).
Nuestro grupo ha propuesto que las
paramiosinas inhiben la producción de mediadores complementarios de inflamación
en la interfase hospedero-cisticerco, es decir, que desempeñan un papel
inmunomodulador de la respuesta del hospedero (46[L148] , 49[L149] ). El cisticerco puede evitar el
reclutamiento de células hacia la interfase para disminuir la confrontación con
su hospedero humano o porcino. Por lo anterior, la TPmy se ha convertido en un
candidato para el desarrollo de una vacuna en contra de la cisticercosis.
Cabe mencionar que la paramiosina es
también candidato para el desarrollo de una vacuna contra infecciones
helmínticas tales como esquistosomosis (23[L150] , 48[L151] , 76[L152] , 77[L153] , 81[L154] , 84[L155] ) y filariasis (51[L156] , 52[L157] ,
70[L158] ). Además, se puede inducir protección
contra Schistosoma japonicum con un
anticuerpo monoclonal IgE anti-paramiosina (71[L159] ) y se ha sugerido que la respuesta
inmune a la paramiosina se relaciona con la resistencia natural a la
esquistosomosis en humanos (15[L160] ). Incluso, se ha logrado producir
anticuerpos anti-paramiosina en ratón al vacunar con fragmentos de DNA que
codifican para paramiosina de Schistosoma japonicum (120[L161] ).
Algunos resultados obtenidos en el laboratorio del Dr. Laclette muestran que la
inmunización con TPmy recombinante induce protección en contra de la
cisticercosis murina (Apéndice 2). Recientemente se ha encontrado que la
inmunización con DNA de TPmy puede inducir protección contra la infección por
el cisticerco de T. crassiceps (Laclette, comunicación personal).
Finalmente, se ha encontrado que un anticuerpo monoclonal dirigido contra un
antígeno de superficie de 14 kDa de Onchocerca
microfilariae reconoce una molécula que parece ser la paramiosina en un
extracto de gusano adulto (13[L162] ).
Para
caracterizar la interacción de la paramiosina con la colágena y el C1q a nivel
submolecular, en nuestro laboratorio se han preparado una serie de
construcciones plasmídicas para la expresión recombinante de diferentes
fragmentos de paramiosina, así como de
la molécula completa. Cada uno de los fragmentos recombinantes ha sido
expresado, purificado en cantidad suficiente (del orden de miligramos) y
probado en experimentos de unión a colágena y C1q, así como de inhibición del
complemento. Cabe hacer notar que esta estrategia es posible gracias a que
disponemos de clonas de cDNA, conteniendo la secuencia codificadora completa de
TPmy (49[L163] ).
Desde los primeros ensayos se determinó que la
interacción con C1q es a través del extremo amino-terminal de la paramiosina.
Por lo cual, en nuestro grupo se han realizado cinco series más de
construcciones de expresión, que han permitido localizar el sitio de unión con
C1q en fragmentos peptídicos cada vez menores, siempre asociado al extremo
amino de la TPmy. El número total de construcciones de expresión exitosas
obtenidas para el gene de TPmy se aproxima a 30. Se ha logrado expresar TPmy en
cantidades preparativas incluso en sistemas eucarióticos glicosilantes. En la
actualidad se tiene una idea razonable de la región de la TPmy que se une al
C1q y este proyecto del grupo se encuentra en una situación investigativa
especialmente interesante (Laclette, comunicación personal).
La
expresión de TPmy recombinante también ha permitido estudiar hacia que regiones
de la proteína se dirige la respuesta inmune humoral y celular del hospedero.
En estos estudios se utilizaron algunos de los fragmentos recombinantes
mencionados arriba. Los ensayos de Western blot en los cuales se enfrentan
sueros de pacientes con cisticercosis con cada uno de los fragmentos
recombinantes, indican que los anticuerpos reaccionan principalmente con el
extremo carboxilo-terminal de la TPmy, mientras que la respuesta celular de los
sanos muestra una preferencia por el extremo amino-terminal (Apéndice 1). Estos
resultados sugieren que el parásito oculta la región que une C1q al
reconocimiento por anticuerpos. Recientemente se ha utilizado la técnica de
“phage display” para la caracterización de secuencias epitópicas dentro de la
TPmy (30[L164] ).
El caso anterior es un ejemplo de la aplicación de
la ingeniería genética para identificar las regiones de una molécula que son
relevantes en su interacción con otras moléculas. Debido a que la paramiosina
es un antígeno natural e inmunodominante es especialmente interesante
determinar cuáles son las regiones de la molécula que interaccionan con el
sistema inmune. Este estudio puede ayudarnos a comprender qué características
debe reunir una molécula para ser inmunodominante o inmunogénica.
10. La
paramiosina como antígeno protector
La inmunización con
paramiosina induce protección contra la esquistosomosis (23[L165] ,
77[L166] ,
81[L167] ,
101[L168] )
y contra la filariasis (52[L169] ,
70[L170] ).
Incluso el DNA codificante de paramiosina induce protección contra S. japonicum (121[L171] )
y se ha inducido protección en cerdos contra la infección por S. japonicum (11[L172] ).
La
paramiosina también puede inducir protección heteróloga. La Pmy de Caenorhabditis elegans induce protección contra Brugia malayi (70[L173] ) y lo mismo se ha sugerido de Lumbricus terrestris contra Schistosoma japonicum (118[L174] ); algo similar se ha encontrado en el
laboratorio del Dr. Laclette, ya que la paramiosina de T. solium induce protección parcial contra T. crassiceps (Apéndice 2). Se ha propuesto que además de la protección de acuerdo
al número de adultos de S. mansoni,
también induce reducción en la formación de granulomas generados por huevos (35[L175] ).
Existe evidencia que
sugiere que la respuesta inmune contra
paramiosina se correlaciona con resistencia en humanos a esquistosomosis
(15[L176] )
y oncocercosis (104[L177] ).
La evidencia respecto al mecanismo
protector que induce la inmunización con paramiosina es interesante, especialmente
por la polarización que fue descubierta en ratón entre la respuesta Th1 y Th2.
Se sabe que la paramiosina
induce protección contra
S. mansoni o B. malayi junto con hipersensibilidad de tipo tardío o DTH (70[L178] , 101[L179] ),
y que provoca la liberación de linfocinas activadoras de macrófagos contra S. mansoni (77[L180] , 101[L181] );
esto sugiere un mecanismo tipo Th1. En otro sentido, se induce protección contra S. japonicum con un anticuerpo monoclonal IgE y se induce
citotoxicidad contra esquistosómulas cuando se incuba con eosinófilos (40[L182] ); esto sugiere un mecanismo tipo Th2.
Estos datos sugieren que la resistencia contra esta clase de parásitos tiene,
en parte al componente celular.
V.
OBJETIVO DE PROYECTO:
El objetivo general de esta tesis es
contribuir a la caracterización de la respuesta inmune que el ser humano y el
ratón desarrollan contra la paramiosina de la T. solium.
Objetivos
particulares:
1)
Inicialmente se estudió la respuesta humoral y celular del humano con
cisticercosis en contra de la TPmy; con el objeto de determinar si la respuesta
humoral y celular de los pacientes mostraba una preferencia de reconocimiento
hacia alguna región de la TPmy, se expresaron en bacteria cuatro productos
recombinantes de la TPmy: la proteína completa, el tercio amino-terminal, el
tercio central y el tercio carboxilo-terminal. Todos ellos fueron purificados
prácticamente a homogeneidad usando una técnica de cromatografía de afinidad
(Apéndice 1), y puestos a reaccionar con sueros de pacientes humanos, o fueron
usados para estimular células de sangre periférica de pacientes en un sistema
de proliferación de linfocitos in vitro.
2)
Debido a que no existe una vacuna establecida contra la cisticercosis evaluamos
la capacidad de la TPmy para inducir protección en contra de la cisticercosis
en el modelo murino. Además, se decidió estudiar la respuesta humoral y celular
del ratón en contra de la TPmy; en concreto, se determinó si la respuesta
humoral y celular del ratón mostraba una preferencia de reconocimiento hacia
una región de la TPmy. Para ello, se emplearon los mismos cuatro productos
recombinantes de la TPmy. Se inmunizaron ratones con la proteína completa y,
los tercios fueron puestos a reaccionar con sueros de los ratones inmunizados,
o fueron usados para estimular células de bazo en un sistema de proliferación
de linfocitaria.
VI. HIPÓTESIS
Dado
que la paramiosina genera protección contra la esquistosomosis y la filariasis,
induce protección contra la cisticercosis. Esto es a través de un perfil de
respuesta inmune tipo Th1 que genera protección contra el cisticerco de T.
crassiceps en el hospedero murino.

