2.-LEYES PONDERALES Y
TEORÍA ATÓMICA DE DALTON. ESTEQUIOMETRÍA DE LA REACCIÓN
QUÍMICA
INTRODUCCION
La química es la parte de la ciencia que se encarga de estudiar, por un lado, la composición de la materia, por otro lado las propiedades de la misma, y también, los cambios que a veces experimenta la materia cuando unas sustancias se transforman en otras.
Esta última parte es fundamental desde el punto de vista tecnológico. Para poder verlo en un ejemplo, imaginemos que necesitamos una pieza de plomo para solucionar un problema tecnológico. El plomo no se encuentra en la naturaleza como tal. Hay un mineral que se llama galena cuyo contenido en sulfuro de plomo es muy alto. Todo esto implica un conocimiento de propiedades de la materia, para reconocer a la misma en la naturaleza, y conocimiento de su composición, para saber que de ahí quizá podamos sacar plomo.
Pero el problema no termina aquí, sino que empieza, ya que żcomo sacamos el plomo de sulfuro de plomo? Gracias a que la química estudia las transformaciones que experimentan los compuestos, sabemos que el sulfuro de plomo a gran temperatura con una fuerte corriente de aire (oxígeno), podremos transformarlo en óxido de plomo(II), y que éste mezclado con carbono a alta temperatura nos permitirá obtener definitivamente el plomo.
PbS + O2 -> PbO + SO2 PbO + C -> Pb + CO2
No hace falta ser muy inteligente para ver que en la primera reacción de desprende dióxido de azufre, y en el segundo caso dióxido carbono, ambos gases contaminantes; Esto implica chimeneas. con esto quiero hacer remarcar que el desarrollo tiene un coste medioambiental, y que un simple trozo de plomo puro implica un poco de contaminación. Tenemos que ser conscientes de ello.
Tratemos ahora de ver la diferencia entre una transformación física y una transformación química como la analizada anteriormente.
Veamos una serie de ejemplos
1) Disolvemos sal en agua.
2) Evaporamos agua.
3) A un vaso con ácido clorhídrico le echamos un trozo de cinc.
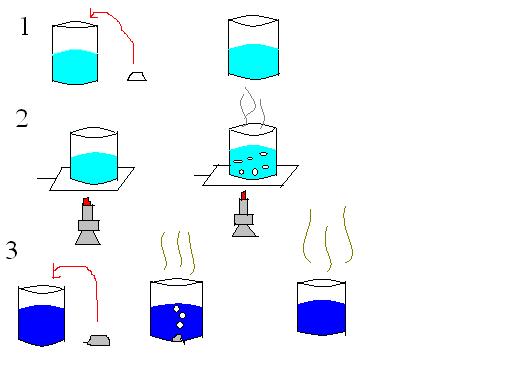
Los dos primeros procesos son procesos físicos ya que no hay destrucción de sustancia. En el primer caso la sal se disuelve en el agua, pero sigue ahí, de hecho, si bebemos ese agua notamos que está salada. En el segundo caso es otro proceso físico, obtenemos vapor de agua, que sigue siendo agua, no hay por lo tanto transformación de materia. En el tercer caso si hay destrucción de materia; Tal como observamos en el dibujo, echamos cinc a un vaso con ácido clorhídrico, e instantaneamente empiezan a aparecer unas burbujas que son hidrógeno, sustancia que antes no existía, y al final no queda nada de ácido clorhídrico y cinc, sólo el hidrógeno que está en el aire y el líquido que es una disolución de cloruro de cinc.
HCl + Zn -> ZnCl2 + H2
Todas las sustancias que hay en la naturaleza podemos clasificarlas en base a 3 propiedades físicas:
a) Punto de fusión.
b) Punto de ebullición.
c) Densidad.
Sería como el DNI, cada sustancia tendría al menos uno de esos tres valores diferentes.
Vamos a hacer una clasificación de los sistemas materiales. Distinguiremos primero entre mezcla homogenea y mezcla heterogenea.
En la mezcla heterogenea podemos distinguir a simple vista sus componentes, mientras que en la mezcla homogenea no. Una paella de arroz o un trozo de granito sería un ejemplo de sistema heterogeneo; En la primera fácilmente distinguimos el arroz de los guisantes, del pimiento... y en el granito también podemos distinguir fácilmente el cuarzo (cristalitos transparentes) de los feldespatos (blanco) y de la mica (negra). En cambio, un vaso de café negro, o un vaso de leche son mezclas homogeneas; ambos tienen muchos componentes que nosotros no podemos distinguir a simple vista.

Granito

Leche
También podremos distinguir entre compuestos y elementos. Digamos que todos los compuestos tienen fórmula química, como el agua(H2O), la sal(NaCl), el ácido clorhídrico (HCl), la cafeína, etc. De los elementos decir que son los que aparecen en la tabla periódica, y la combinación de estos da los compuestos.
A modo de resumen decir que la combinción de elementos da los compuestos, y la combinación de estos pueden dar lugar a mezclas homogeneas o mezclas heterogeneas. El hidrógeno, el oxígeno, el sodio y el cloro son elementos, los dos primeros forman agua mientras que los tercero y cuarto forman sal, ambos compuestos que al mezclarse dan agua salada que es una mezcla homogenea.
LA LEY DE CONSERVACIÓN DE LA MASA
Enunciada por Lavoisier (siglo XVIII), dice: En una reacción química, la masa de las sustancias que intervienen permanecen invariable, es decir, que la masa de los reactivos es igual a la masa de los productos.
Esta ley parece una obviedad si pensamos que la masa mide la cantidad de materia, y que a lo largo de una reacción química, que es un proceso en el cual unos compuestos se transforman en otros, no puede haber ni desaparición de materia, ni aparición de ésta; Estaríamos hablando de magia si afirmásemos lo contrario.
Pero en la época que fue enunciada, en los albores de la química, trajo cierta controversia ya que había fenómenos que parecían indicar lo contrario. Veamos tres ejemplos:
a) Empezamos por uno fácil, un incendio de un bosque es una reacción química de combustión, y en principio, todo nos hace pensar que el bosque tenía más masa que las cenizas que quedan después.
b) Los químicos de la época de Lavoisier observaban que cuando calentaban un metal como el hierro, éste ganaba en peso.
c) Si en nuestro laboratorio hacemos reacciónar Zn y HCl, veremos que no acaba de cumplirse la ley enunciada por Lavoisier.
HCl + Zn -> ZnCl2 + H2
El hidrógeno lo vamos recogiendo en la probeta invertida. El gas desplaza al agua.
żQue es lo que sucede? Pues que no hemos tenido en cuenta todos los participantes en la reacciones químicas anteriores. En el incendio forestal nos habíamos olvidado de la gran cantidad de humo desprendido a lo largo del mismo que son productos de la reacción, en el caso del hierro, el "engorde" el mismo se debe a que está reaccionando con el oxígeno que toma de la atmósfera, el cual no lo hemos tenido en cuenta, y se está formando un óxido de hierro, y en el último caso, nos estábamos olvidando del hidrógeno que se ha ido formando y que no hemos tenido en cuenta.
Por lo tanto, la ley de conservación de la masa enunciada por Lavoisier se cumple y hemos de tenerla siempre en cuenta.
LA LEY DE LAS PROPORCIONES DEFINIDAS
Enunciada por Proust (ańo 1801) dice que cuando dos ó más elementos se combinan para formar un determinado compuesto, lo hacen siempre en las mismas proporciones.
Imaginen que cuando habitualmente cocinamos una paella utilizamos 1 kg de arroz y 1/4 kg de pimientos entre otros ingredientes. Si el número de invitados a nuestra casa fuera el doble, a los 2 kg de arroz le acompańaría 1/2 kg de pimientos para que nuestra paella tuviera el saber que habitualmente tiene, y si otro día cocinamos 1/2 kg de arroz, la cantidad de pimiento tendría que ser de 1/8 kg. Las proprociones entre ambos ingredientes tendrían que respetarse para que la paella no variara de sabor.
Pasando a un ejemplo químico, en el monóxido de carbono, 12 g de C se combinan con 16 de O, y si fueran 24 g de C se combinarían con 32 g de O. Si por ejemplo tuvieramos los mismos elementos pero en otra proporción, por ejemplo 12 g de C con 32 g de O, ya tendríamos otro compuesto que en este caso sería el dióxido de carbono, con propiedades químicas diferentes; Así mientras que el primero es letal nada más respirarse, el segundo es más inactivo, más denso qu el oxígeno y el causante, por ejemplo, del efecto invernadero.
CO
CO2
TEORÍA ATÓMICA DE DALTON
La teoría atómica enunciada por John Dalton (1766-1844) se basa en las siguientes hipótesis (no vamos a enunciarla exactamente como él lo hizo para facilitar su comprensión):
1) La materia está formada por unas partículas muy peqeuńas que son átomos indivisibles e indestructibles, de tal manera que un átomo es la última división de la materia a la que podemos llegar. Los átomos serían los "ladrillos" de la materia.
2) Los átomos de un mismo elemento químico son iguales en masa y en propiedades, es decir los átomos de oxígeno son iguales a los que haya de oxígeno en el "otro extremo del universo".
3) Los átomos de diferentes elemento químico serán diferentes en masa y en propiedades. Esto quiere decir que los átomos de O y C, por ejemplo, nunca serán iguales bajo ninguna circunstancia.
4) Los átomos se unen para formar atomo compuestos (hoy conocidos como moléculas) en una relación de número entero sencillo. EL supuso que la relación iba a ser 1:1 ó 1:1:1. Así por ejemplo el ácido clorhídrico, el agua o el ácido sulfúrico los escribiría como HCl, HO y HSO.
5) Una reacción química es una reordenación de los átomos en la molécula. Así por ejemplo, esto sería en dibujo la siguiente reacción química:
HCl + Zn -> ZnCl2 + H2
Como vemos en el dibujo, las bolas azules, que son átomos de cloro, se combinaban inicialmente con las pequeńitas y blancas que son átomos de hidrógeno, formando el ácido clorhídrico. Los átomos de Zn, que son las bolas grandes y grises aparecen solos. Después de la reacción química, vemos que se ha producido una recombinación, de tal modo que los átomos de hidrógeno se combinan entre ellos (las bolitas pequeńas blancas), mientras que cada átomo de Zn (bola grande y gris) se combina con dos átomos de cloro (bolas azules).
La idea de molécula fue introducida por Avogadro (1776-1856).
Como dijimos, Dalton pensabe que las proporciones en las que iban los átomos en las moléculas era siempre 1:1, la más fácil que podía imaginar; En esa época no había medios para comprobar dichas proporciones, y era lógico pensar en una relación sencilla.
Avogadro fue quien vio que no tenía por que ser tales proporciones gracias a unos trabajos que había hecho Gay Lussac en relación a reacciones químicas con gases
HCl, H2O, H2SO4
LA REACCIÓN QUÍMICA
Una reacción química es un proceso en el cual, dos ó más sustancas entran en contacto, se destruyen transformándose en otras diferentes.
Para que una reacción química se produzca, las sustancias deben estrar en contacto físico. Las sustancias que teníamos al principio y que se destruyen en dicho proceso se llaman reactivos, mientras que las sustancias nuevas que aparecen se llaman productos
En la reacción química representada en el dibujo, vemos como el ácido clorhídrico y el cinc se ponen en contacto (reactivos), reaccionan desapareciendo y convirtiéndose en dos sustancias nuevas (productos) que son el hidrógeno, que se desprende del cinc, y la disolución de cloruro de cinc que es lo que queda en el vaso.
Hay una forma de representar la reacción química que no es con dibujos. Esta forma se llama ecuación química.A la izquierda se colocan los reactivos y a la derecha los productos, separadas unos de otros por una flecha que me indica el sentido de la reacción química.
HCl + Zn --> ZnCl2 + H2 Tanto los reactivos como los productos están separados entre si por signo se sumar.
PRINCIPIO DE CONSERVACIÓN DE LA MASA
En una reacción química la masa permanece constante, es decir, la masa delos reactivos tiene que ser igual a la masa de los productos. Cualquier otra cosa significaría que aparacería o desaparecería materia, lo cual no puede ser cierto; Ua reacción química no es un proceso mágico, y aunque unas sustancias se transformen en otras, la cantidad de materia permanece constante a lo largo de todo el proceso. Esto es lo que se llama principio de conservación de la masa
Analicemos desde este punto de vista la reacción del apartado anterior.
HCl + Zn --> ZnCl2 + H2
Si nos fijamos atentamente notaremos que sucede algo extrańo.
-al principio había un átomo de hidrógeno mientras que entre los productos contamos dos. Aparece un átomo de hidrógeno que antes no existía.
-Lo mismo sucede para el Cl, al final hay dos átomos, luego aparece uno que antes no estaba.
-De acuerdo con nuestro ejemplo, para que sólo el zn respeta el principio de conservación de la masa ya que partíamos de un átomo de Zn y al final también hay uno.
żNo se cumple el principio de conservación de la masa? No se trata de eso, simplemente que la ecuación no estaba ajustada, y por lo tanto hay que ajustarla, colocarle números delante de las fórmulas correspondientes a las sustancias para que termine cuadrando todo.
2 HCl + Zn --> ZnCl2 + H2
Ya está la ecuación ajustada. Ahora sí cuadra todo. Los números que se colocan delante de las fórmulas se llaman coeficientes estequiométricos y me informa de las proporciones en las cuales reaccionan las sustancias químicas.
Igual que cuando vamos a cocinar una paella, los ingredientes guardan una serie de proporciones y no va 1 kg de cada cosa (1kg de arroz + 1 kg de sal + 1kg de ajo, etc), en las reacciones químicas sucede lo mismo. en nuestro ejemplo anterior, por cada átomo de cinc, reaccionan 2 moléculas de ácido clorhídrico (en este caso en una proporción doble como indica el coeficiente estequiométrico)
SIGNIFICADO DEL COEFICIENTE ESQUIOMÉTRICO
El coeficiente estequiméetrico que aparece como resultado de ajustar una reacción química nos indica cuantas moléculas se combinan de cada especie y cuantas se obtienen.
Así, del ejemplo anterior cabe deducirse que por cada átomo de cinc reaccionan dos moléculas de ácido clorhídrico, y se obtienen una molécula de cloruro de cinc y otra de hidrógeno, o
por cada 2 átomos de cinc reaccionan cuatro moléculas de ácido clorhídrico, y se obtienen dos moléculas de cloruro de cinc y otras dos de hidrógeno, o
por cada 10 átomos de cinc reaccionan 20 moléculas de ácido clorhídrico, y se obtienen 10 moléculas de cloruro de cinc y otras 10 de hidrógeno, o
Ejercicios
1) Indicar cuales de las siguientes ecuaciones químicas están ajustadas y cuales no. Ajusten las que no lo estén e indique cuantas moléculas de cada compuesto se combinan entre si, y cuantas moléculas de cada producto resultan al final.
HCl + Fe -> FeCl3 + H2 NaCl + H2SO4 -> Na2SO4 + HCl FeO + CO -> Fe + CO2 NaOH + H2SO4 -> Na2SO4 + H2O
PESOS ATÓMICOS Y MOLECULARES
Si queremos reproducir una buena receta de una comida en nuetra cocina, tendremos que cuidar que los ingredientes estén en las proporciones perfectas.
aalgo parecido nos ocurre en un laboratorio con las reacciones químicas, pero nos topamos con un problema inicial que luego se va a complicar un poco, y es como medir la masa de los cuerpos que son tan pequeńos como los átomos y moléculas.
Necesitamos crear una nueva unidad de masa que se ajuste a nuestras necesidades, y esta es la U.M.A. (unidad de masa aómica). Una U.M.A. se corresponde con la masa de 1/12 parte del isótopo 12 del carbono.
Así la masa atómica sería la masa de un átomo medida con esta unidad.
Las masa atómicas o pesos atómicos de todos los elementos los podemos encontrar en la tabla periódica. Si por ejemplo, la masa atómica del azufre es 32, resulta que la masa de 1 átomo de azufre es 32 veces más grande que la masa de 1/12 parte del isótopo del carbono 12.
La masa molecular será la masa de una molécula entera y se hallará sumando las masas atómicas de todos los átomos que componen dicha molécula.
Ejemplo: Masa atómica de H2SO4
1 at de S · 32 U.M.A. = 32 U.M.A.
2 at de H · 1 U.M.A. = 2 U.M.A.
4 at de O · 16 U.M.A. = 64 U.M.A.
Sumamos todo: La masa atómica de ácido sulfúrico será: 32 + 2 + 64 = 98 U.M.A.
Ejercicio
1) Hallar con ayuda de una tabla periódica las masas moleculares o atómicas de las siguientes especies químicas.
HCl
Fe
FeCl3
H2
NaCl
Na2SO4
HCl
FeO
CO
CO2
NaOH
H2O
EL CONCEPTO DE MOL. UNA NUEVA INTERPRETACIÓN DE LA ECUACIÓN QUÍMICA
Si bien hemos solucionado el tema cuantitativo a la hora de trabajar en el laboratorio,, este trabajo tendrá que ser sumamente complicado porque las cantidades con las que trabajaríamos serían demasiado pequeńas.
Para solucionar esto surge el concepto de mol. Un mol es la masa de 6.02 · (10)23 partículas.
Así por ejemplo, 1 mol de HCl es la masa de 6.02 · (10)23 moléculas de HCl, ó 1 mol de H2 es la masa de 6.02 · (10)23 moléculas de H2, o 1 mol de H2SO4 es la masa de 6.02 · (10)23 moléculas de H2SO4
żResultará grande o pequeńa dicha cantidad? Esa cantidad coincide con la masa molecular expresada en gramos.
Así, 1 mol de HCl es la masa de 6.02 · (10)23 moléculas de HCl, es decir, 36.5 g ó 1 mol de H2 es la masa de 6.02 · (10)23 moléculas de H2, es decir, 2g, o 1 mol de H2SO4 es la masa de 6.02 · (10)23 moléculas de H2SO4, es decir, 98 g
El número que procura dicha "feliz coincidencia" es 6.02 ·(10)23, al que se le llama Número de Avogadro
De acuerdo con esto, también podríamos definir mol como la masa molecular de una sustancia expresada en gramos.
Así, de cara al trabajo en el laboratorio, podríamos interpretar la siguiente reacción de la siguiente manera:
2 HCl + Zn --> ZnCl2 + H2
Podríamos decir que:
- 2 Moles de HCl reaccionan con 1 de Zn para dar 1 mol de ZnCl2 y otro mol de H2
- 72 g de HCl (2 · 36 g) reaccionan con 65 g de Zn para dar 135 g de ZnCl2 y 2 g de H2.
Estas sí son ya cantidades que puedo medir en un laboratorio, y son cantidades que se ajustan a las proporciones establecidas por la ecuación química.
Ejercicios
1) Una vez haya ajustado las siguientes ecuaciones químicas, indique cuantos gramos se combinan de reactivos y cuantos se obtienen de productos.
HCl + Fe -> FeCl3 + H2 NaCl + H2SO4 -> Na2SO4 + HCl FeO + CO -> Fe + CO2 NaOH + H2SO4 -> Na2SO4 + H2O
REACTIVO LIMITANTE
En realidad, no siempre se ajustan perfectamente todas las cantidades de los reactivos que intervienen en la reacción química. Para ahorrar tiempo, lo que se hace es ajustar la cantidad del reactivo más caro. Este se echa en su cantidad justa mientras que el otro reactivo que echa en exceso con la certeza de que la reacción va a finalizar cuando todo el reactivo cuya cantidad he calculado se acabe. A este reactivo que marca el final de la reacción, cuyo cálculo he hecho, se le llama reactivo limitante.
En este contexto, vamos a abordar un problema que podríamos tener en el laboratorio.
Vamos a ver una serie de pasos que hemos de seguir para abordar un problema de estas características. Hay un modo mucho más rápido y directo de hacer lo que vamos a estudiar, pero para evitar errores, vamos a empezar por este método más secuendiado.
El problema sería: Calcular la cantidad de hidrógeno que obtendré si hago reaccionar 6.5 g de Zn con una cantidad en exceso de HCl. El termómetro del laboratorio me indica una temperatura de 20ş C, mientras que el barómetro una presión de 760 mm Hg
1) El primer paso consistiría en ajustar la ecuación química.
2 HCl + Zn --> ZnCl2 + H2
2) Una vez ajustada la ecuación tendremos que pasar a moles el dato de nuestro reactivo limitante. Siempre que tangamos una conversión g moles o moles g, acudiremos a la expresión:
n = m / Pmol
de donde tendremos que despejar lo que vayamos a necesitar. Si el reactivo limitante es líquido (no en nuestro ejemplo), tendremos un dato de volumen en vez de un dato de masa. En dicha circunstancia, nos darán también la densidad de dicha reactivo, y hallaremos previamente la masa despejándola de la fórula de la densidad. Una vez hallada la masa, podremos seguir adelante con el cálculo de moles. Vayamos a nuestro caso.
n = m / Pat = 6.5 g / 65g/mol = 0.1 moles de Zn
3) El siguiente paso sería hacer una "regla de 3" de acuerdo con las proprociones establecidas por los coeficientes estequiométricos entre el reactivo limitante y lo que tenmos que hallar.
Si 1 mol de Zn da 1 mol de H2, entonces 0.1 g de Zn daría x moles de H2
1 mol Zn / 1mol H2 = 0.1 mol Zn / x moles H2
Esta proporción 1:1 resulta fácil, obtendríamos 0.1 moles de hidrógeno.
4) El último paso consiste en dar la solución en la unidad adecuada. Aquí tendremos 3 posibilidades distintas:
-Que el producto sea un gas, como es nuestro caso. Tendríamos que expresar el dato de moles en volumen que es como se describen los gases. para ello utilizaremos la acuadión de estado de los gases idelas, y dado que siempre podremos medir la temperatura y la presión en el laboratorio, podremos despejar el volumen sin problemas una vez hayamos resuelto el apartado 3 (hallar número de moles)
P · V = n · R · T; V = n · R · T
P
-Si el producto es un sólido, simplemente tendremos que hallar la masa justo al contrario de como lo hicimos en el apartado 1, con la precaución de que el peso molecular a sustituir ahora no es el del reactivo limitante sino el del producto cuya cantidad estamos hallando.
n = m; m = n · Pmol
Pmol
-Si se trata de un líquido, primero tendremos que hallar la masa como justo lo hemos hecho en el quión anterior, y con el dato de densidad del líquido, podremos hallar finalmente el volumen. Reccuerde que los líquidos se expresan en volumen.
n = m; m = n · Pmol
Pmol
d = m; m = d · V ;
V
V = m
d
Si en el margen izquierdo no tienes el mapa de la web pulsa aqui y luego busca esta sección en ella
|
EJERCICIOS. 1) żQue es la quimica? 2) Explique que diferencias hay entre un proceso quimico y un proceso físico. Cite un par de ejemplos donde se pongan de manifiesto dichas diferencias. 3) żQue diferencias hay entre un sistema material homogeneo y otro heterogeneo? 4) Escriba dos ejemplos, uno de sistema material homogeneo, y otro de sistema material heterogeneo, indicando los compuestos y elementos que componen dichos sistemas materiales. 5) żQue diferencia shay entre un compuesto y un elemento. 6) Enuncie la ley de conservación de la masa y ponga un ejemplo. 7) Según la ley de las proporciones definidas, si con 16 g de oxígeno se han combinado 2 g de hidrógeno en la formación de agua, żCuántos gramos de hidrógeno se combinarían con 48 gramos de oxígeno? 8) żQué es una molécula? 9) Interprete con un dibujo las siguientes reacciones químicas según la teoría atómica de Dalton.
CaCO3 = CaO + CO2
CH4 + O2 = CO2 + H2O
10)Hallar las masas moleculares de los siguientes compuestos. NaF CO1 NO2 H2SO4 Li CaSO4 Ca 11) Calcule la cantidad de hidrógeno que obtendríamos si hacemos reaccionar 3 g de Fe con una cantidad en exceso de HCl. Los datos de presión y temperatura en el laboratorio son de 760 mm de Hg y 18 ş C. HCl + Fe -> FeCl3 + H2 12) Calcule la cantidad de óxido cálcico que obtendríamos a partir de 40 g de carbonato cálcico. CaCO3 -> CaO + CO2 13) Determinar el volumen de dióxido de azufre a 25şC y 1 atmósfera de presión que se obtendría al tostar 8 g de mineral blenda (mineral rico en ZnS) si éste contiene un 60% de ZnS ZnS + O2 -> SO2 + ZnO |