Pilhas Secas
O tipo de bateria usada em vários flashes, rádios portáteis, e outros dispositivos foi inventado por um químico francês em 1865, e ficou conhecida como pilha-seca. A bateria de George Leclanche continha uma solução condutiva de sal amoníaco, um terminal negativo de zinco e um terminal positivo de carbono. Leclanche converteu o que antigamente era uma solução líquida condutiva em uma pasta rígida, fazendo uma bateria portátil e de fácil manuseio. Sua bateria foi um sucesso comercial imediato, principalmente por sua conveniência e pelos seus materiais baratos.
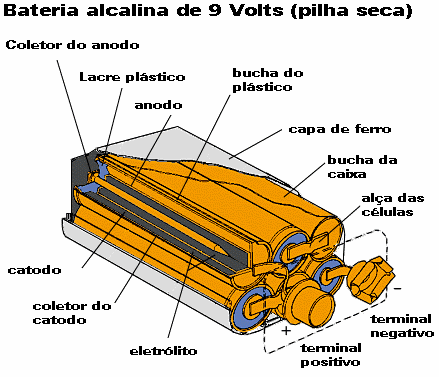
O zinco e as pilhas alcalinas
O zinco é o material ânodo mais comum, por causa das suas boas propriedades eletroquímicas, disponibilidade e baixo custo. A voltagem de pilhas deste tipo é de 1,5 Volts. Tanto as baterias de zinco-carbono como as baterias alcalinas são produzidas como pilhas "secas", porque seu eletrólito é imobilizado como uma pasta, ou é contido num separador poroso.
A pilha de zinco-carbono, ou pilha de Leclanche, era o único sistema amplamente disponível até mais ou menos 1940. Pelo início da década de 80, ainda era uma bateria popular, usada em flashes, rádios e brinquedos.
A pilha alcalina é uma variação da pilha de Leclache, que utiliza a mesma química básica dos eletrodos, mas um eletrólito diferente. Ela é um pouco mais cara, mas provê um desempenho bastante melhorado, mais força e vida útil. São usadas em gravadores, calculadoras, rádios portáteis e outros aparelhos.
Funcionamento
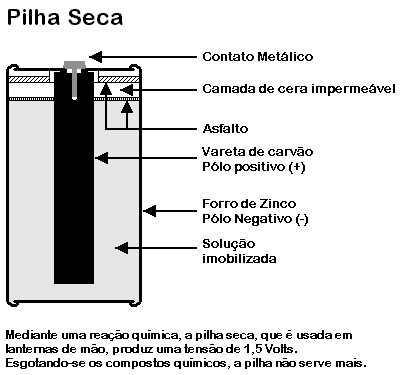
Uma pilha seca comum é formada por um eletrodo de zinco, que também é o invólucro metálico da pilha, e um eletrodo central e cilíndrico de carvão. Separando os dois eletrodos há uma pasta gelatinosa à base de cloreto de amônio, que constitui o eletrólito da pilha.
Ao se completar o circuito elétrico externo, a corrente é criada através da ação do eletrólito sobre o zinco, que constitui o eletrodo ou pólo negativo do aparelho. A ação química liberta átomos de hidrogênio que se acumulam sobre a superfície do pólo positivo. Essa ação, chamada polarização, faz diminuir progressivamente a produção de corrente, acabado por tornar a pilha inútil ou "descarregada". Para retardar o máximo possível os efeitos dessa polarização, costuma-se colocar entre o eletrólito e o eletrodo positivo uma camada de mistura despolarizante, no caso, geralmente, bióxido de manganês. Os átomos de hidrogênio formados pela reação química combinam-se com os átomos de oxigênio do bióxido de manganês, formando água e despolarizando, assim, a pilha.
Tipos/Aplicações
As pilhas podem ser classificadas em secas e úmidas. As secas tem como eletrólito uma pasta enrijecida. Já o eletrólito das pilhas úmidas é uma solução líquida .
As pilhas secas são usadas para produzir correntes pequenas, em serviços contínuos, ou quando se deseja corrente moderada e serviço intermitente. Assim, são usadas em baterias de rádios portáteis, telefones, telegrafia, operação automática de aparelhos controladas por relé, campainhas, lanternas, serviços de sinalização, transceptores do tipo handy-talk. As pilhas úmidas são empregadas em instalações estacionárias para sinalização, telefonia, galvanoplastia, e para alimentação de medidores elétricos. Seu uso é muito difundido também em serviços de laboratório.
CONHEÇA UM POUCO SOBRE / LINKS E REFERÊNCIA BIBLIOGRÁFICAS
/