

|
|
|
Introdução
Capacidade calorífera ou capacidade térmica de um corpo é a razão entre a quantidade de calor a ele cedida e a elevação de temperatura correspondente:
![]()
O procedimento usado foi o " princípio da igualdade das trocas de calor" ou método das misturas.
Quando corpos isolados de meio externo trocam calor entre si, a quantidade de calor cedida por um corpo é igual a quantidade recebida pelo outro corpo.
As trocas de calor irão acontecer até que a temperatura dos corpos entre em equilíbrio:
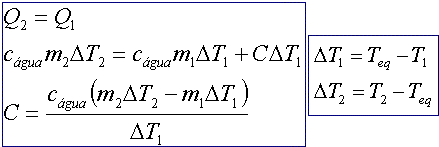
Experiência
Objetivos:
Determinar a capacidade térmica do calorímetro (C) pelo método das misturas: água em temperatura ambiente (1) e água quente (2) .
Tendo o valor da capacidade térmica do calorímetro, determinar o calor específico do álcool, tendo como valor para a água 1Cal/oC.
Material:
Calorímetro;
Termômetro;
Balança;
cuba de metal;
becker com água;
becker com álcool.
Procedimentos:
Colocar uma massa (m1) de água na temperatura ambiente no calorímetro;
Colocar uma massa (m2) de água quente.
Medir a variação da temperatura de equilíbrio a cada 5 min;
Tabelas e resultados:
cágua = 1,0 cal/oC
m1 = ______g
T1 = ____ºC
DT1 = ____ºC
m2 = _____g
T2 = _____ºC
DT2 = ____ºC
Teq = _____ºC
Obtendo a capacidade térmica do calorímetro:
m2 cágua DT2 = m1 cágua DT1 + C DT1
C = _______ cal/ºC
Quantidade de calor do calorímetro:
Qcal = (m2 + m1) cágua DT + C DT
Qcal = _____ cal
Obtendo o calor específico do álcool:
Qcal = Qálcool málcool = ____
_____ = málcool c DTálcool Tálcool = ___
c = ___cal/ºC
Teq = _____
- Analisar os resultados obtidos
- Fazer uma conclusão