

|
|
|
Calor específico de uma substância é a quantidade de calor necessário para elevar 1ºC a temperatura da unidade de massa dessa substância, sem mudar o seu estado.
As quantidades de calor do sistema em equilíbrio dentro de um calorímetro pode ser dado como:
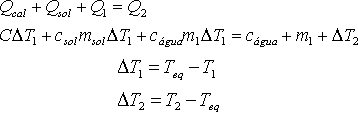
Qcal = quantidade de calor do calorímetro (recebe calor)
Qsol = quantidade de calor do sólido (recebe calor)
Q1 = quantidade de calor da água fria (recebe calor)
Q2 = quantidade de calor da água quente (doa calor)
C = capacidade térmica
Teq = temperatura de equilíbrio
T1 = temperatura da água fria, do sólido ou temperatura ambiente
m1 = massa da água fria
msol = massa do sólido
csol = calor específico do sólido
cágua = calor específico da água
T2 = temperatura da água quente
m2 = massa da água quente
Experiência
Objetivos
Obter a capacidade térmica do calorímetro (C)
Obter o calor específico (csol) de 4 materiais diferentes
Materiais utilizados
cuba de metal, calorímetro de isopor e becker;
termômetro;
água ;
4 tipos de sólidos (Latão, Alumínio, Chumbo e Cobre);
aquecedor de água;
balança.
Procedimentos
Obter a capacidade térmica do calorímetro (23,6 cal/0C)
Medir a massa da água fria (m1) e dos sólidos (msol) e suas temperaturas (T1 - temperatura ambiente);
Colocar os materiais no calorímetro;
Aquecer mais uma massa de água (m2) e medir sua temperatura (T2 - temperatura da água quente);
Colocar e massa de água quente no calorímetro;
Esperar a temperatura entrar em equilíbrio (Tq);
Repetir esses procedimentos com todos os sólidos.
Tabelas / Resultados
|
materiais |
m1 |
T1 |
m2 |
T2 |
Teq |
msol |
DT1 |
DT2 |
c |
c'* |
E %** |
|
Latão |
|
|
|
|
|
|
|
|
|
|
|
|
Alumínio |
|
|
|
|
|
|
|
|
|
|
|
|
Chumbo |
|
|
|
|
|
|
|
|
|
|
|
|
Cobre |
|
|
|
|
|
|
|
|
|
|
|
* valor tabelado da capacidade térmica
** Erro experimental: E% = |(c-c')/c'|*100%
Analisar os resultados obtidos
Fazer uma conclusão