



Res ulta
sorprendente que Isaac Newton haya descubierto algo en su vida,
ya que era el representante auténtico del profesor distraído.
Se dice que siempre medía el tiempo de cocción del huevo que
tomaba en el desayuno. Una mañana su sirvienta lo encontró
parado frente a un cazo con agua hirviente, sostenía un huevo en
la mano y miraba fijamente el reloj ¡que había puesto en el
fondo del cazo!
ulta
sorprendente que Isaac Newton haya descubierto algo en su vida,
ya que era el representante auténtico del profesor distraído.
Se dice que siempre medía el tiempo de cocción del huevo que
tomaba en el desayuno. Una mañana su sirvienta lo encontró
parado frente a un cazo con agua hirviente, sostenía un huevo en
la mano y miraba fijamente el reloj ¡que había puesto en el
fondo del cazo!


Bueno, parece que han descubierto un elemento nuevo, aunque hay rumores de que ya se conocía desde hace mucho tiempo...Aquí detallo sus características:
Símbolo: Mu

Peso atómico: 50 Kg. valor correspondiente a la media ponderada, ya que se conocen muchos isótopos de geometría y tamaños muy diversos. Las dimensiones atómicas del isótopo más preciado son 90x60x90 (Armstrongs)
Historia: el elemento fue descubierto por el alquimista Adán quien, entusiasmado por el descubrimiento, abordó rápidamente su estudio. No obstante, poco después, convencido de su peligrosidad y difícil manejo, abandonó sus investigaciones. Algo se ha avanzado desde entonces, pero aún es mucho lo que resta por saberse de este elemento. Hasta los 14 años se la encuentra químicamente puro; de ahí en adelante, y hasta los 80, se encuentra mezclado con gran cantidad de barnices, carbón, ceras, sustancias grasas y cremas de olor insoportable.
Estado natural: se encuentra en la naturaleza en grandes cantidades, pudiendo adoptar diversos colores: negras, blancas, amarillas,...
Propiedades físicas: elemento muy inestable, tiene un periodo de semidesintegración de 28 días. Es muy frágil y nada maleable. Hierve con el menor pretexto y se congela sin razón alguna. Pierde su agua de cristalización (lágrimas) a la menor contrariedad. Es tan volátil que se evapora cuando le da la putísima gana.
Propiedades químicas: se trata de un elemento quimicamente muy reactivo. Captan azufre (es decir, se sulfuran) con suma facilidad. Se acomplejan muy fácilmente, incluso con los ligandos más extraños. Poseen gran afinidad por el oro, plata y piedras preciosas. Es un reductor muy enérgico (reducen la riqueza del varón rápidamente). En principio, y dado su sabor amargo, se le considera un ácido; sin embargo, en otros casos, se asemeja más al NaOH (bien por lo de sosa, bien por lo de cáustica); es decir, se comporta como un anfótero. Aunque la valencia más común es 1 (por falta de reactivo), puede actuar con valencias muy superiores: poligamorfia. Desaloja a todos los elemento de su familia. Pertenece al grupo de tierras raras.
Marcha analítica del reconocimiento: ensayos organolépticos: olor en general agradable; sabor indescriptible (dicen); tacto macizo; precipita rápidamente frente a un millonario. Confunden al mejor químico: son capaces de hacer ver lo negro, blanco.
Usos: muy ornamental; excelente como afrodisíaco. Precauciones: dada su gran reactividad, sobre todo en caliente, deben manipularse con sumo cuidado. En manos inexpertas, pueden resultar explosivas. A altas concentraciones (más de dos unidades juntas), resultan especialmente peligrosas. En caso de intoxicación por contacto con una excesiva cantidad (más de 3 en una noche) se recomienda reposo absoluto y dosis masivas de vitaminas y reconstituyentes.
 Toxicidad Química y Riesgo
Toxicidad Química y Riesgo
Nosotros oímos y leemos un montón actualmente
sobre los peligros de los productos químicos. ¿Qué debe creer
una persona ?
?
La vida no está libre de riesgos; nosotros corremos muchos riesgos cada día. Decidimos ir en bicicleta más que conducir, incluso aunque hay una probabilidad de muerte de un 10 por mil más por ir en bicicleta que en coche. Alguna gente puede decidir fumar, incluso aunque ello aumenta su probabilidad de desarrollar un cáncer en un 50%. Tomar decisiones que afectan a nuestra salud es algo que hacemos diariamente sin pensarlo.
¿Pero acerca de riesgos de productos químicos?
La evaluación de riesgo es llevada a cabo exponiendo ratas, por
ejemplo, a un producto químico y entonces observarlos por si hay
signos de daño. Para limitar el gasto y el tiempo necesarios,
las cantidades administradas son cientos o miles de veces mayores
que lo que un a persona podría encontrarse. Una vez
que los datos del animal están disponibles, la interpretación
de éstos conlleva algunas hipótesis. ¿Si una sustancia es dañina
en animales, es necesariamente dañina para el hombre?¿Cómo
puede una gran dosis para un pequeño animal ser transportada a
una pequeña dosis para el hombre? Como señaló en el siglo XVI
el médico suizo Paracelso, "La dosis hace el veneno".
Todas las sustancias son tóxicas en algunos organismos en alguna
extensión y la diferencia entre beneficio y daño es un problema
de graduación.
a persona podría encontrarse. Una vez
que los datos del animal están disponibles, la interpretación
de éstos conlleva algunas hipótesis. ¿Si una sustancia es dañina
en animales, es necesariamente dañina para el hombre?¿Cómo
puede una gran dosis para un pequeño animal ser transportada a
una pequeña dosis para el hombre? Como señaló en el siglo XVI
el médico suizo Paracelso, "La dosis hace el veneno".
Todas las sustancias son tóxicas en algunos organismos en alguna
extensión y la diferencia entre beneficio y daño es un problema
de graduación.
El método estándar para evaluar toxicidad química aguda es el del valor LD50, la cantidad de una sustancia por kilogramo peso que es letal al 50% de las ratas.
Cómo respondemos a un riesgo está fuertemente influenciado por familiaridad. La presencia de cloroformo en los suministros municipales de agua ha causado protestas en algunas ciudades, a pesar de que tiene una toxicidad aguda menor que la de la aspirina. Algunos alimentos, ingredientes naturales son más tóxicos que los aditivos de comidas sintéticos, pero los ingredientes son ignorados porque los alimentos son familiares.
 Espectroscopia de absorción atómica
Espectroscopia de absorción atómica
Cabe esperar que un cuerpo que brilla, emita un
espectro continuo de radiación electromagnética. Sin embargo, a
principios del siglo XIX un científico alemán, Josef von
Fraunhofer, observó que el espectro visible del sol contenía en
real idad varias bandas oscuras. Investigadores
posteriores se dieron cuenta que las bandas eran el resultado de
la absorción de ciertas longitudes de onda por átomos menos
calientes en la "atmósfera" sobre la superficie solar.
Los electrones de estos átomos estaban en estado basal, y absorbían
radiación a longitudes de onda que correspondían a la energía
que necesitaban para excitarse y alcanzar estados energéticos más
altos. Un estudio de tales espectros "negativos" llevó
al descubrimiento del helio. Los estudios espectrales de este
tipo siguen teniendo gran importancia en la cosmoquímica: el
estudio de la composición química de las estrellas.
idad varias bandas oscuras. Investigadores
posteriores se dieron cuenta que las bandas eran el resultado de
la absorción de ciertas longitudes de onda por átomos menos
calientes en la "atmósfera" sobre la superficie solar.
Los electrones de estos átomos estaban en estado basal, y absorbían
radiación a longitudes de onda que correspondían a la energía
que necesitaban para excitarse y alcanzar estados energéticos más
altos. Un estudio de tales espectros "negativos" llevó
al descubrimiento del helio. Los estudios espectrales de este
tipo siguen teniendo gran importancia en la cosmoquímica: el
estudio de la composición química de las estrellas.
En 1955 dos grupos de científicos se percataron
que el método de absorción podría servir para detectar la
presencia de elementos en concentraciones muy bajas. Cada
elemento tiene un espectro de absorción específico que
corresponde a las distintas separaciones entre los niveles energéticos
de sus átomos. Cuando la luz de una fuente potente atraviesa una
muestra vaporizada de un elemento, se absorben las longitudes de
onda específicas que corresponden a las diversas 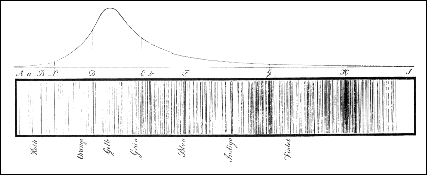 separaciones energéticas. Cuanto mayor
es la concentración de los átomos, mayor es la proporción de
la luz que se absorbe. La sensibilidad de este método es
extremadamente alta, y es fácil determinar las concentraciones
de partes por millón; algunos elementos se pueden determinar con
una precisión de partes por mil millones. La espectroscopia de
absorción atómica se ha convertido en una herramienta analítica
de rutina en química, metalurgia, geología, medicina,
investigación forense y muchos otros campos científicos. Lo único
que se requiere es el movimiento de electrones de un nivel energético
a otro.
separaciones energéticas. Cuanto mayor
es la concentración de los átomos, mayor es la proporción de
la luz que se absorbe. La sensibilidad de este método es
extremadamente alta, y es fácil determinar las concentraciones
de partes por millón; algunos elementos se pueden determinar con
una precisión de partes por mil millones. La espectroscopia de
absorción atómica se ha convertido en una herramienta analítica
de rutina en química, metalurgia, geología, medicina,
investigación forense y muchos otros campos científicos. Lo único
que se requiere es el movimiento de electrones de un nivel energético
a otro.
 Alcaloides
Alcaloides
Además del aminíaco, una base débil, hay un gran número de compuestos orgánicos que contienen nitrógeno llamados aminas que son bases débiles también. En los primeros tiempos de la química orgánica, las aminas básicas derivaban de fuentes naturales que eren conocidas como "álcalis vegetales", pero ahora son conocidos como alcaloides. El estudio de los alcaloides proporcionó la mayor parte de los estímulos para el crecimiento de la química orgánica en el siglo XIX y deja hoy un área fascinante de investigación.
Los alcaloides varían en estructura, desde uno simple hasta lo más complejo. El olor del pescado podrido, por ejemplo, es causado por la metilamina, un sencillo "pariente" del amoníaco en el cual uno de los hidrógenos del amoníaco es sustituido por un grupo metilo.
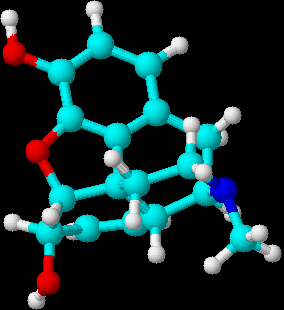 Morfina
Morfina
Algunos alcaloides tienen importantes propiedades biológicas y algunos de los agentes farmacéuticos usados hoy son derivados de aminas. La morfina y otros alcaloides de la adormidera de opio, por ejemplo, son usados para calmar el dolor; la atropina de la planta Atropa belladonna, es usada como agente antiespasmódico en el tratamiento de la colitis; y efedrina de la planta china Ephedra sinica es usada como broncodilatador y descongestionante.


Una de las preguntas más seductoras planteadas a principios
del siglo XX fue la siguiente: ¿cómo se combinan los átomos
para formar moléculas? Un gran precursor en el estudio de los
enlaces fue Gilbert N. Lewis, criado en una pequeña granja de
Nebraska. Lewis sugirió en 1916 que los electrones externos se
podían visualizar como ubicados en los vértices de un cubo
imaginario en torno al núcleo. Un átomo deficiente en
electrones que necesitase llenar los 8 vértices del cubo podría
compartir aristas con otro átomo para completar su octeto.
Como suele ocurrir con una gran parte de las ideas revolucionarias, muchos de los químicos de la época rechazaron la propuesta. El muy conocido químico Kasimir Fajans comentó:
Decir que cada uno de los dos átomos puede alcanzar capas electrónicas cerradas compartiendo pares de electrones, equivale a afirmar que un hombre y su esposa, si tienen dos dólares en una cuenta bancaria mancomunada, y cada uno seis dólares más en sendas cuentas bancarias individuales, entonces tienen ocho dólares cada uno.
 Gasolina de petróleo
Gasolina de petróleo
Los depósit os de gas natural y de petróleo
constituyen la fuente más grande de alcanos. Estos depósitos
proceden de la descomposición de plantas y animales,
inicialmente de origen marino. El gas Natural está
constituido principalmente por metano, pero también contiene
etano, propano, butano e isobutano. El petróleo es una
mezcla compleja de hidrocarburos que debe ser refinado en
fracciones antes de que pueda ser utilizado.
os de gas natural y de petróleo
constituyen la fuente más grande de alcanos. Estos depósitos
proceden de la descomposición de plantas y animales,
inicialmente de origen marino. El gas Natural está
constituido principalmente por metano, pero también contiene
etano, propano, butano e isobutano. El petróleo es una
mezcla compleja de hidrocarburos que debe ser refinado en
fracciones antes de que pueda ser utilizado.
La refinación comienza por destilación
de crudo en tres cortes principales: gasolina, queroseno y gasóleo.
Finalmente, la destilación a presión reducida da aceites
lubricantes y grasas, y queda un indestilable residuo de asfalto.
La destilación de crudo es sólo el primer paso en la producción de gasolina. Como tiene un alto porcentaje de alcanos no ramificados y es por tanto un combustible malo, los químicos del petróleo han diseñado varios métodos para producir combustibles de mayor calidad. Uno de estos métodos, craqueo catalítico, consiste en tomar el corte del queroseno y "craquearlo" en moléculas más pequeñas adecuadas para el uso en la gasolina.
![]()
 Amalgama de mercurio en los dientes
Amalgama de mercurio en los dientes
Muchos de nosotros tenemos mercurio en la boca, en forma de empastes dentales. Los empastes consisten en una amalgama, una mezcla homogénea de un metal líquido y diversos metales sólidos. Típicamente, la amalgama dental tiene composiciones del orden siguiente: mercurio, plata, estaño, zinc y cobre. La mezcla suave se coloca en la caries dental excavada mientras todavía es una suspensión de partículas de los metales sólidos en mercurio. En la cavidad, los átomos de mercurio se infiltran en la estructura metálica para dar una amalgama sólida. A medida que la reacción se produce, hay una ligera expansión que mantiene el empaste en su lugar.
El mercurio es un elemento muy tóxico. Sin embargo, al amalgamarse con metales con metales sólidos su presión de vapor disminuye, por lo que no presenta el mismo grado de peligrosidad que el mercurio líquido puro. El veredicto de la American Dental Association es que los empastes de mercurio son muy seguros, pero algunas personas alegan que, incluso a niveles muy bajos, el mercurio que se desprende de los empastes representa un peligro. El verdadero problema es que no disponemos de un sustituto aceptable por el momento. Actualmente, los investigadores intentan sintetizar un material capaz de unirse químicamente a la superficie del diente y que sea lo suficientemente resistente para soportar las enormes presiones que aplicamos a nuestros dientes posteriores.
A medida que la cremación se hace mñas común, en particular en los países muy poblados, se hace necesario reconocer el potencial de la contaminación por mercurio. Durante la incineración de los cadáveres la amalgama de mercurio se descompone y libera vapor de mercurio en la atmósfera. Por tanto, los controles ambientales de las emisiones de los crematorios son un nuevo motivo de preocupación.
Si te interesa aportar alguna anécdota curiosa o alguna
noticia interesante, o, sin más, tu opinión acerca de algo
relacionado con la química, mándamelo