|
COLEGIO POLITECNICO "EDUCADORA ELENA ROJAS" DEPTO DE CIENCIAS NATURALES FISICA CONTENIDOS 4to Año Medio (Electivo) |
|
|
COLEGIO POLITECNICO "EDUCADORA ELENA ROJAS" DEPTO DE CIENCIAS NATURALES FISICA CONTENIDOS 4to Año Medio (Electivo) |
|
|
(Actualización 14 de Junio 2009)
TEORIA CINETICO MOLECULAR
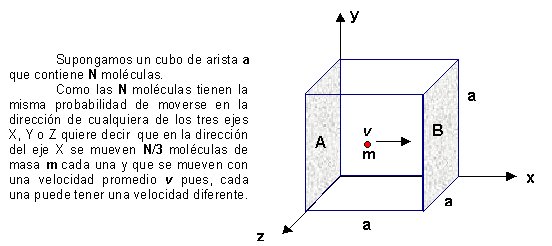
Como los choques de las moléculas entre sí o contra las paredes del recipiente son elásticos, es decir, que tanto la energía cinética como la cantidad de movimiento de la molécula m antes y después del choque no varían en magnitud sino sólo en sentido. De tal manera que la cantidad de movimiento de la molécula m antes del choque es mv y después del choque es - m v. Se produce en la dirección del eje X una variación de la cantidad de movimiento igual a : mv - (- m v ) = 2 mv , por cada molécula. Como existen N/3 moléculas que se mueven en la dirección del eje X chocando contra la pared A y B, la variación de la cantidad de movimiento en esa dirección será: 2 mv N/3 .
Por otro lado, sabemos que la variación de la cantidad de movimiento es igual al impulso F t , en que F es la fuerza con que chocan las N/3 moléculas contra la pared A y t es el tiempo que demora cada molécula en recorrer la distancia 2 a, entre dos choques sucesivos de la misma molécula contra la pared A.
Luego:
![]() ; pero
; pero
![]() y reemplazando
en la ecuación anterior
y reemplazando
en la ecuación anterior
resulta que:
![]() y si despejamos la fuerza
F se obtiene que :
y si despejamos la fuerza
F se obtiene que :
![]()
Conociendo la fuerza F que actúa sobre la cara A de superficie a2, se puede calcular la presión P sobre esta cara debida al choque de las moléculas contra ella.
Sabemos que: P = fuerza / superficie , se obtiene que:
![]()
Pero a3 es el volumen total V que se ha considerado, por lo tanto, la presión viene dada por la expresión:
![]()
Además, siendo m la masa de una de las moléculas y N el número total de ellas, el producto N m representa la masa total M del gas encerrado en el volumen V.
Por la tantoutilizando estas expresiones, la ecuación anterior puede escribirse en la forma
:![]()
Y como ![]() es
la densidad (d ), resulta que
es
la densidad (d ), resulta que
![]()
Y la expresión
![]()
Puede escribirse como:
![]()
en que ![]() es la energía
cinética media de cada molécula y
es la energía
cinética media de cada molécula y
![]()
es la energía cinética de las N moléculas del gas,
luego:![]()
pero ![]() y reemplazando
en la ecuación anterior, nos queda:
y reemplazando
en la ecuación anterior, nos queda:
![]()
Como n y R son constantes, la ecuación anterior nos indica que "la temperatura del gas sólo depende de la energía cinética molecular". Es independiente de la presión y del volumen del gas.
Si la temperatura del gas es de 0 kelvin, la energía cinética molecular es nula.
La expresión
![]() puede escribirse
como:
puede escribirse
como: ![]()
Donde la razón ![]() se
denomina constante de Boltzmann, de donde se obtiene que
se
denomina constante de Boltzmann, de donde se obtiene que
![]() o bien,
o bien,
![]()
lo que también se puede escribir como
![]()